题目内容
4.6g钠和一定量的水完全反应后得到100mL的NaOH溶液,求:
(1)标准状况下放出氢气的体积是多少?
(2)所得NaOH溶液的物质的量浓度是多少?
(3)若将所得NaOH溶液加水稀释到200mL,则所得溶液的物质的量浓度是多少?
(1)标准状况下放出氢气的体积是多少?
(2)所得NaOH溶液的物质的量浓度是多少?
(3)若将所得NaOH溶液加水稀释到200mL,则所得溶液的物质的量浓度是多少?
考点:化学方程式的有关计算,物质的量浓度的相关计算
专题:计算题
分析:发生反应:2Na+2H2O=2NaOH+H2↑,根据n=
计算4.6gNa的物质的量,根据方程式计算生成氢气、氢氧化钠的物质的量,
(1)根据V=nVm计算氢气的体积;
(2)根据c=
计算所得NaOH溶液的物质的量浓度;
(3)根据稀释定律,稀释前后NaOH的物质的量不变,根据c=
计算计算稀释后溶液浓度.
| m |
| M |
(1)根据V=nVm计算氢气的体积;
(2)根据c=
| n |
| V |
(3)根据稀释定律,稀释前后NaOH的物质的量不变,根据c=
| n |
| V |
解答:
解:4.6gNa的物质的量=
=0.2mol,
2Na+2H2O=2NaOH+H2↑
2 2 1
0.2mol n(NaOH) n(H2)
故n(NaOH)=
=0.2mol n(H2)=
=0.1mol
(1)标况下生成氢气的体积=0.1mol×22.4L/mol=2.24L,
答:标况下生成氢气为2.24L.
(2)所得NaOH溶液的物质的量浓度=
=2mol/L,
答:所得NaOH溶液的物质的量浓度为2mol/L.
(3)根据稀释定律,稀释前后NaOH的物质的量不变,故稀释后溶液浓度=
=1mol/L,
答:稀释后氢氧化钠溶液的浓度为1mol/L.
| 4.6g |
| 23g/mol |
2Na+2H2O=2NaOH+H2↑
2 2 1
0.2mol n(NaOH) n(H2)
故n(NaOH)=
| 0.2mol×2 |
| 2 |
| 0.2mol×1 |
| 2 |
(1)标况下生成氢气的体积=0.1mol×22.4L/mol=2.24L,
答:标况下生成氢气为2.24L.
(2)所得NaOH溶液的物质的量浓度=
| 0.2mol |
| 0.1L |
答:所得NaOH溶液的物质的量浓度为2mol/L.
(3)根据稀释定律,稀释前后NaOH的物质的量不变,故稀释后溶液浓度=
| 0.2mol |
| 0.2L |
答:稀释后氢氧化钠溶液的浓度为1mol/L.
点评:本题考查方程式的有关计算、物质的量浓度计算等,比较基础,注意对物质的量浓度公式的理解与灵活应用.

练习册系列答案
相关题目
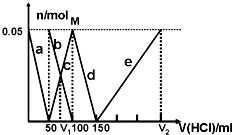 某Na2CO3、NaAlO2的混合溶液中逐滴加入1mol?L-1的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+离子的物质的量与加入盐酸溶液的体积变化关系如图所示.则下列说法不正确的是( )
某Na2CO3、NaAlO2的混合溶液中逐滴加入1mol?L-1的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+离子的物质的量与加入盐酸溶液的体积变化关系如图所示.则下列说法不正确的是( )| A、原混合溶液中的CO32-与AlO2-的物质的量之比为1:2 |
| B、V1:V2=1:4 |
| C、M点时生成的CO2为0mol |
| D、a曲线表示的离子方程式为:AlO2-+H++H2O═Al(OH)3↓ |
已知:将Cl2通入适量KOH溶液中,产物中可能有KCl,KClO,KClO3,且
的值与温度高低有关.当n(KOH)=a mol时,下列有关说法错误的是( )
| c(Cl-) |
| c(ClO-) |
A、若某温度下,反应后
| ||||||
B、参加反应的氯气的物质的量等于
| ||||||
C、改变温度,反应中转移电子的物质的量ne的范围:
| ||||||
D、改变温度,产物中KClO3的最大理论产量为
|
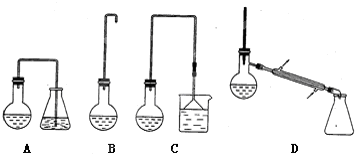
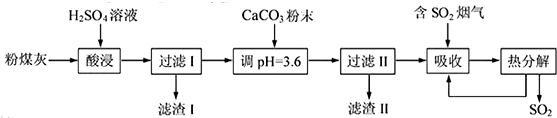
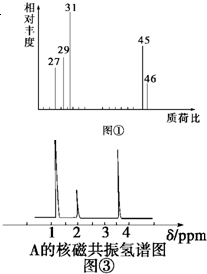 为测定某有机化合物A的结构,进行如下实验:
为测定某有机化合物A的结构,进行如下实验: