题目内容
13.下列叙述正确的是( )| A. | 饱和石灰水中加入少量CaO,恢复至原温度后,溶液的pH不变 | |
| B. | 稀醋酸加水稀释,醋酸电离程度增大,溶液的pH减小 | |
| C. | 盐酸中滴加氨水至中性,溶液中的溶质只有氯化铵 | |
| D. | 室温时pH=3的硫酸和pH=11的氨水等体积混合后,溶液的pH小于7 |
分析 A、饱和石灰水中加入氧化钙会与水反应生成氢氧化钙,析出晶体后溶液仍是饱和溶液离子浓度不变;
B、醋酸是弱电解质,加水稀释促进电离,平衡状态下离子浓度减小;
C、当盐酸和氨水恰好中和生成NH4Cl时,铵根离子水解呈酸性;
D、根据两种溶液中H+和OH-的关系以及氨水为弱电解质的性质,判断反应后酸碱的过量,进而判断反应后溶液的酸碱性.
解答 解:A、温度不变,Ca(OH)2的溶解度不发生变化,故饱和石灰水中c(OH-)的浓度不变,所以pH不变,故A正确;
B、向稀醋酸中加水时,醋酸的电离平衡正向移动,醋酸的电离程度增大,但c(H+)减小,故pH增大,故B错误;
C、当盐酸和氨水恰好中和生成NH4Cl时,由于铵根离子水解呈酸性,若使溶液呈中性,应继续向溶液中加入氨水,故溶液中的溶质是NH4Cl和NH3•H2O,故C错误;
D、pH=3的盐酸中c(H+)=10-3mol/L,pH=11的氨水中c(OH-)=10-3mol/L,两种溶液H+与OH-离子浓度相等,但由于氨水为弱电解质,不能完全电离,则氨水浓度大于盐酸浓度,反应后氨水过量,溶液呈碱性,则所得溶液的pH>7,故D错误.
故选A.
点评 本题考查了酸碱反应的溶液酸碱性判断,弱电解质稀释溶液PH变化,饱和溶液的离子浓度分析,胶体性质的应用,题目难度中等.

练习册系列答案
相关题目
4.下列有机物分子中,所有的碳原子可能不处于同一平面上的是( )
| A. | CH2=CH-CH3 | B. | C6H5-CH=CH2 | C. | C6H5-CH3 | D. | CH2=CH2 |
1.NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A. | 在密闭容器中加入l.5mol H2和0.5molN2,充分反应后可得到NH3分子数为NA | |
| B. | 一定条件下,2.3g的Na完全与O2反应生成3.6g产物时失去的电子数为0.1NA | |
| C. | 7.1gCl2与足量的氢氧化钠溶液反应转移的电子数为0.2NA | |
| D. | 标准状况下,22.4L的CCl4中含有的CCl4分子数为NA |
8.如图表示水溶液中c(H+)和c(OH-)的关系,下列判断正确的是( )
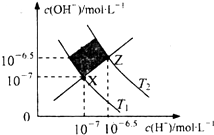

| A. | XZ线上任意点均表示溶液的pH=7 | |
| B. | 图中T1>T2 | |
| C. | M区域对应溶液中大量存在:Fe3+、Na+、C1-、SO42- | |
| D. | Z点对应的可能是CH3COOH和CH3COONa的混合液,且c(CH3COO-)=c(Na+) |
18.在溶液中能大量共存,且加入稀硫酸时,有气体生成的是( )
| A. | Na+、Ag+、CO32-、Cl- | B. | K+、Ba2+、SO42-、Cl- | ||
| C. | Na+、K+、CO32-、Cl- | D. | Na+、K+、Cl-、SO42- |
5.下列叙述I和II均正确并有因果关系的是( )
| 选项 | 叙述I | 叙述II |
| A | 用酸度计测定SO2和CO2饱和溶液的pH,前者pH小 | 结论:说明H2SO3酸性强于H2CO3 |
| B | SiO2是酸性氧化物 | SiO2不与任何酸溶液反应 |
| C | 配制SnCl2溶液时,先将SnCl2溶于适量的稀盐酸中,再用蒸馏水稀释,保存时再在试剂瓶中加入少量的锡粒 | 抑制Sn2+水解,并防止Sn2+被氧化为Sn4+ |
| D | 浓硝酸具有强氧化性 | 应保存在棕色玻璃试剂瓶中 |
| A. | A | B. | B | C. | C | D. | D |
2.短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示,这四种元素的原子最外层电子数之和为20.则下列说法不正确的是( )
| X | Y | |||
| W | Z |
| A. | 最高价氧化物的水化物的酸性:X<Z | |
| B. | 原子半径大小:Y<W | |
| C. | X的非金属性大于Y | |
| D. | W的最高价氧化物的水化物具有两性 |
3.下列离子方程式正确的是( )
| A. | 硫酸铜溶液与氢氧化钡溶液反应:SO${\;}_{4}^{2-}$+Ba2+═BaSO4↓ | |
| B. | 漂白粉溶液在空气中发生的反应:Ca2++2ClO-+CO2+H2O═2HClO+CaCO3↓ | |
| C. | 碳酸钙溶解于盐酸中:CO32-+2H+═CO2↑+H2O | |
| D. | 氯化铁溶液与碘化钾溶液反应:Fe3++2Iˉ═Fe2++I2 |
