题目内容
下列叙述正确的是( )
| A、丁达尔效应是区分溶液和胶体的一种常用物理方法 |
| B、氯化钠溶液蒸发结晶时,必须将蒸发皿中的液体蒸干才能停止加热 |
| C、实验室可用KOH稀溶液除去NaCl溶液中混有的少量MgCl2杂质 |
| D、测定某溶液的pH,常用干燥洁净的玻璃棒蘸取该溶液滴在润湿的pH试纸上 |
考点:胶体的重要性质,试纸的使用,物质的分离、提纯和除杂
专题:化学实验基本操作
分析:A.胶体有丁达尔效应;
B.蒸发皿中出现较多的固体就停止加热;
C.除杂不能引入新的杂质;
D.pH试纸不能润湿.
B.蒸发皿中出现较多的固体就停止加热;
C.除杂不能引入新的杂质;
D.pH试纸不能润湿.
解答:
解:A.胶体有丁达尔效应,溶液无丁达尔效应,故A正确;
B.不能等液体蒸干才停止加热,只要蒸发皿中出现较多的固体就停止加热,故B错误;
C.引入了新的杂质钾离子,故C错误;
D.pH试纸不能润湿,润湿相当于稀释了溶液,故D错误.
故选A.
B.不能等液体蒸干才停止加热,只要蒸发皿中出现较多的固体就停止加热,故B错误;
C.引入了新的杂质钾离子,故C错误;
D.pH试纸不能润湿,润湿相当于稀释了溶液,故D错误.
故选A.
点评:本题考查化学实验的基本操作,题目难度不大,注意相关基本实验操作的实验注意事项.

练习册系列答案
相关题目
下列有关大小关系的判断中,肯定正确的是( )
| A、常温下,将甲酸钠和适量盐酸混合,若所得的溶液恰好呈中性,则粒子间存在大小关系:c(Na+)>c(HCOO-)>c(HCOOH)>c(H+)=c(OH-) |
| B、将amol/L的Na2RO3溶液与bmol/L的NaHRO3溶液等体积混合,若离子间存在大小关系:c(Na+)>c(HRO3-)>c(RO32-)>c(OH-)>c(H+),则有:a<b |
| C、若KHA溶液呈酸性,则离子间一定存在大小关系:c(Na+)>c(HA-)>c(A2-)>c(H+)>c(OH-) |
| D、向硝酸银溶液中逐滴滴加物质的量浓度相等的氯化钾和铬酸钾的混合溶液,若先产生白色的氯化银沉淀,则有:Ksp(AgCl)<Ksp(Ag2CrO4) |
下列基态原子的电子排布图中,正确的是( )
A、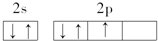 |
B、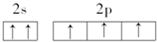 |
C、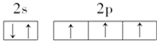 |
D、 |
将4mol A气体和2mol B气体在2L的密闭容器中混合并在一定条件下发生如下反应2A(g)+B(g)?2C(g)△H<0,4s后反应达到平衡状态,此时测得C的浓度为0.6mol/L,下列说法中正确的是( )
| A、反应过程中,当A、B、C的物质的量浓度之比为2:1:2时,反应即达到平衡状态 |
| B、达平衡后若升高温度,C的浓度将增大 |
| C、达平衡后若增大压强,A的转化率降低 |
| D、4 s内用物质B表示的反应速率为0.075 mol/(L?s) |
将标准状况下a L HCl(g)溶于100g水中,得到的盐酸的密度为b g?cm-3,则该盐酸的物质的量浓度是( )
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
下列事实中,不能用来比较主族元素金属性或非金属性强弱的是( )
| A、化合价高低 |
| B、氢化物的稳定性 |
| C、元素在周期表中的位置 |
| D、最高价氧化物对应水化物的酸性或碱性强弱 |
根据元素周期表和元素周期律的下列推断,其中错误的是( )
| A、铍(Be)的原子失电子能力比镁弱 |
| B、砹(At)的氢化物不稳定 |
| C、砷酸(H3AsO4)比磷酸的酸性强 |
| D、硫酸锶(SrSO4)是难溶于水的白色固体 |