题目内容
17.
 (1)FeCl3具有净水作用,但腐蚀设备,FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示)2Fe3++Fe=3Fe2+.
(1)FeCl3具有净水作用,但腐蚀设备,FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示)2Fe3++Fe=3Fe2+.(2)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3,完成NaClO3氧化FeCl2的离子方程式:
□ClO3-+□Fe2++□6H+=□Cl-+□Fe3++□3H2O.
(3)高铁酸钾是一种氧化、吸附、絮凝、助凝、杀菌、除臭为一体的新型高效多功能绿色水处理剂,具有良好的应用前景.其生产工艺如图1所示

①实验室模拟工业流程中过滤操作用到的主要玻璃仪器有漏斗、烧杯、玻璃棒.
②在“反应液Ⅰ”中加KOH固体的目的有两个,a是与“反应液Ⅰ”中过量的Cl2继续反应,生成更多的KClO,b是为下一步反应提供反应物;
③用K2FeO4给水消毒、杀菌时得到的Fe3+可以净水,Fe3+净水的原因是Fe3++3H2O?Fe(OH)3(胶体)+3H+(用离子方程式表示).
(4)从环境保护的角度看,制备K2Fe2O4较好的方法为电解法,其装置如图2所示.电解过程中阳极电极反应式为Fe+8OH--6e-═FeO42-+4H2O.
(5)钢铁腐蚀造成很大损失,有资料显示,全世界每年由于腐蚀而造成报废的钢铁高达总产量的三分之一.防止钢铁腐蚀有很多措施,用图3装置放置钢铁腐蚀(烧杯中均有食盐水),X极的电极材料应是A(填字母).
A.锌 B.铜 C.银 D.石墨.
分析 (1)钢铁设备中的Fe会与铁离子反应生成亚铁离子;
(2)氯酸钠氧化酸性的氯化亚铁,则反应物中有氢离子参加,则生成物中有水生成,Cl元素的化合价从+5价降低到-1价,得到6个电子,而Fe元素的化合价从+2价升高到+3价,失去1个电子,根据得失电子守恒,则氯酸根离子的系数为1,Fe2+的系数为6,则铁离子的系数也是6,氯离子的系数是1,根据电荷守恒,则氢离子的系数是6,水的系数是3;
(3)足量Cl2通入和KOH溶液中,温度低时发生反应Cl2+2OH-=Cl-+ClO-+H2O,向溶液I中加入KOH,使氯气完全反应,且将溶液转化为碱性溶液,只有碱性条件下次氯酸根离子才能和铁离子发生氧化还原反应生成高铁酸根离子,除去KCl得到碱性的KClO浓溶液,向碱性的KClO浓溶液中加入90%的Fe(NO3)3溶液,发生反应2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O,得到溶液II,纯化得到湿产品,将湿产品洗涤、干燥得到晶体K2FeO4.
①根据过滤的操作步骤分析所用仪器,玻璃仪器有漏斗、烧杯和玻璃棒;
②KOH和氯气反应生成KClO,除去未反应的氯气,且只有碱性条件下,铁离子才能和次氯酸根离子发生氧化还原反应生成高铁酸根离子;
③Fe3+水解生成的Fe(OH)3胶体粒子能吸附水中的悬浮杂质,可起到净水的作用;
(4)电解时阳极Fe失电子发生氧化反应,电极反应方程式为Fe+8OH--6e-═FeO42-+4H2O;
(5)装置为原电池,若用d装置保护铁,X极的电极材料应比铁活泼.
解答 解:(1)铁离子具有氧化性,钢铁设备中的Fe会与铁离子反应生成亚铁离子,离子方程式是:2Fe3++Fe=3Fe2+,故答案为:2Fe3++Fe=3Fe2+;
(2)氯酸钠氧化酸性的氯化亚铁,则反应物中有氢离子参加,则生成物中有水生成,Cl元素的化合价从+5价降低到-1价,得到6个电子,而Fe元素的化合价从+2价升高到+3价,失去1个电子,根据得失电子守恒,则氯酸根离子的系数为1,Fe2+的系数为6,则铁离子的系数也是6,氯离子的系数是1,根据电荷守恒,则氢离子的系数是6,水的系数是3,配平后离子方程式为:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O,
故答案为:1;6;6H+;1;6;3H2O;
(3)①过滤,玻璃仪器有漏斗作过滤器,烧杯盛放待过滤液、和过滤液,玻璃棒作用为引流,
故答案为:漏斗、烧杯、玻璃棒;
②KOH和氯气反应生成KClO,除去未反应的氯气,且只有碱性条件下,铁离子才能和次氯酸根离子发生氧化还原反应生成高铁酸根离子,所以加入KOH的目的是除去氯气且使溶液为后一步反应提供碱性,
故答案为:为下一步反应提供反应物;
③铁酸钠被还原后的产物Fe3+水解生成的Fe(OH)3胶体粒子能吸附水中的悬浮杂质,可起到净水的作用,Fe3+水解离子方程式为:Fe3++3H2O?Fe(OH)3(胶体)+3H+,
故答案为:Fe3++3H2O?Fe(OH)3(胶体)+3H+;
(4)电解时阳极Fe失电子发生氧化反应,电极反应方程式为Fe+8OH--6e-═FeO42-+4H2O,故答案为:Fe+8OH--6e-═FeO42-+4H2O;
(5)装置为原电池,若用d装置保护铁,X极的电极材料应比铁活泼可以选择锌,故答案为:A.
点评 本题考查了氧化还原反应、原电池和电解池原理、物质的分离与提纯等,题目难度中等,需要学生具有扎实的基础知识与灵活运用知识解决问题的能力,注意基础知识的掌握.

 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案(1)如表列举了不同温度下大气固氮和工业固氮的部分K值.
| 反应 | 大气固氮 N2(g)+O2(g)?2NO(g) | 工业固氮 N2(g)+3H2(g)?2NH3(g) | |||
| 温度/℃ | 27 | 2000 | 25 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |
②分析数据可知:人类不适合大规模模拟大气固氮的原因K值小,正向进行的程度小(或转化率低),不适合大规模生产.
③从平衡视角考虑,工业固氮应该选择常温条件,但实际工业生产却选择500℃左右的高温,解释其原因从反应速率角度考虑,高温更好,但从催化剂活性等综合因素考虑选择500℃左右合适.
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(р1、р2)下随温度变化的曲线,如图所示的图示中,正确的是A(填“A”或“B”);比较р1、р2的大小关系р2>р1.
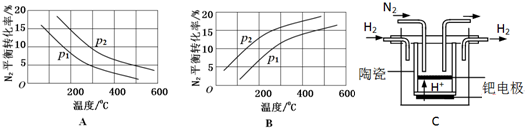
(3)20世纪末,科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现高温常压下的电化学合成氨,提高了反应物的转化率,其实验简图如C所示,阴极的电极反应式是N2+6e-+6H+=2NH3.
(4)近年,又有科学家提出在常温、常压、催化剂等条件下合成氨气的新思路,反应原理为:2N2(g)+6H2O(1)?4NH3(g)+3O2(g),则其反应热△H=+1530kJ•mol-1.
(已知:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1,2H2(g)+O2(g)?2H2O(l)△H=-571.6kJ•mol-1)
| A. | 二氧化硅溶于水显酸性 | |
| B. | 二氧化碳通入水玻璃(Na2SiO3的水溶液)可以得到白色胶状物质 | |
| C. | 因为高温时,二氧化硅与碳酸钠反应放出二氧化碳,所以硅酸的酸性比碳酸强 | |
| D. | 二氧化硅是酸性氧化物,它不溶于任何酸 |
| A. | 13.3% | B. | 26.6% | C. | 20% | D. | ≥20% |
| A. | 若c(CH3COOH)=0.1mol/L,反应后的溶液中:c(CH3COO-)+c(OH-)=c(Na+)+c(H+) | |
| B. | 若c(CH3COOH)=0.1mol/L,反应后的溶液中:c(OH-)>c(CH3COOH)+c(H+) | |
| C. | 若c(CH3COOH)=0.2mol/L,反应后的溶液中:c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+) | |
| D. | 若反应后的溶液呈中性,则:c(CH3COOH)+c(CH3COO-)>0.05mol/L |
| A. | 5 | B. | 9 | C. | 7 | D. | 14 |
| A. | 2mol A+1mol B | |
| B. | 1mol C+1mol D | |
| C. | 2mol C+2mol D | |
| D. | 0.5mol A+0.5mol B+0.5mol C+1mol D |
 用脱脂棉包住0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴几滴水,可观察到脱脂棉剧烈燃烧起来.
用脱脂棉包住0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴几滴水,可观察到脱脂棉剧烈燃烧起来. 学习化学应该明确“从生活中来,到生活中去”的道理.
学习化学应该明确“从生活中来,到生活中去”的道理.