题目内容
下列离子方程式正确的是( )
| A、向NaAlO2溶液中通入足量的CO2气体:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| B、向FeSO4酸性溶液中加入过氧化氢溶液:2Fe2++H2O2+2H+=2Fe3++2H2O |
| C、向溴水中通入SO2气体:SO2+Br2+2H2O=2H++SO42-+2HBr |
| D、FeS加入稀硫酸中:S2-+2H+=H2S |
考点:离子方程式的书写
专题:离子反应专题
分析:A.二氧化碳足量,反应生成碳酸氢根离子;
B.FeSO4酸性溶液中加入过氧化氢溶液发生氧化还原反应生成硫酸铁和水;
C.溴化氢为强电解质应拆成离子形式;
D.硫化亚铁为沉淀应保留化学式.
B.FeSO4酸性溶液中加入过氧化氢溶液发生氧化还原反应生成硫酸铁和水;
C.溴化氢为强电解质应拆成离子形式;
D.硫化亚铁为沉淀应保留化学式.
解答:
解:A.向NaAlO2溶液中通入足量的CO2气体,离子方程式:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,故A错误;
B.向FeSO4酸性溶液中加入过氧化氢溶液,离子方程式:2Fe2++H2O2+2H+=2Fe3++2H2O,故B正确;
C.向溴水中通入SO2气体,反应生成硫酸和氢溴酸,离子方程式:SO2+Br2+2H2O=4H++SO42-+2Br-,故C错误;
D.FeS加入稀硫酸中,离子方程式:FeS+2H+=H2S+Fe2+,故D错误;
故选:B.
B.向FeSO4酸性溶液中加入过氧化氢溶液,离子方程式:2Fe2++H2O2+2H+=2Fe3++2H2O,故B正确;
C.向溴水中通入SO2气体,反应生成硫酸和氢溴酸,离子方程式:SO2+Br2+2H2O=4H++SO42-+2Br-,故C错误;
D.FeS加入稀硫酸中,离子方程式:FeS+2H+=H2S+Fe2+,故D错误;
故选:B.
点评:本题考查常见方程式的书写,明确发生的反应是解题关键,注意化学式的拆分、原子个数守恒、电荷数守恒,题目难度不大.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、Na2O与Na2O2都能与水反应生成碱,它们都是碱性氧化物 |
| B、Na2CO3溶液和NaHCO3溶液都能与CaCl2溶液反应得到白色沉淀 |
| C、钠在常温下不容易被氧化 |
| D、Na2O2可作供氧剂,而Na2O不行 |
短周期元素X、Y、Z原子序数依次增大,X原子的核外电子数与Y原子的最外层电子数相等,Y原子的最外层电子数是内层电子数的3倍,Z的原子半径大于Y,Z与R能形成离子化合物RZ2,且两种离子具有相同的电子层结构.下列判断正确的是( )
| A、X与Y形成的分子中既含有极性共价键又含有非极性共价键 |
| B、X的气态氢化物比Y的气态氢化物稳定 |
| C、X与R、Y与R均能形成阴阳离子数目之比为1:1的化合物 |
| D、R、X、Y三种元素可形成化学式为RXY3、R(X2Y4)2的两种盐 |
下列表达方式正确的是( )
A、碳-12原子
| ||
B、羟基电子式 | ||
C、硫离子结构示意图 | ||
D、CH4S的结构式 |
下列溶液的溶质都是强电解质,这些溶液中的Cl-浓度与50mL 1mol?L-1 MgCl2溶液中的Cl-浓度相等的是( )
| A、150 mL 1 mol?L-1 NaCl溶液 |
| B、75 mL 1 mol?L-1CaCl2溶液 |
| C、150 mL 2 mol?L-1 KCl溶液 |
| D、75 mL 1 mol?L-1AlCl3溶液 |
下列物质为纯净物的是( )
| A、冰醋酸 | B、医用酒精 |
| C、福尔马林 | D、汽油 |
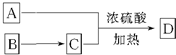 所示转化关系,D的分子式为C10H12O3,A与C反应的化学方程式
所示转化关系,D的分子式为C10H12O3,A与C反应的化学方程式