题目内容
8.在化学反应X+2Y=R+2M中,已知R和M的摩尔质量之比为22:9,当1.6克X与Y恰好完全反应后,生成4.4克R,同时生成M的质量为3.6g克,Y与M的质量之比为16:9,解答此题时使用到的化学定律是质量守恒定律.分析 任何化学反应中都遵循质量守恒定律,根据方程式知,该反应中生成R、M的物质的量之比为1:2,R和M的摩尔质量之比为22:9,则生成4.4克R时同时生成M质量=$\frac{4.4g}{22}$×2×9=3.6g,根据质量守恒定律计算Y质量,然后得出Y与M的质量之比,据此分析解答.
解答 解:任何化学反应中都遵循质量守恒定律,根据方程式知,该反应中生成R、M的物质的量之比为1:2,R和M的摩尔质量之比为22:9,则生成4.4克R时同时生成M质量为:$\frac{4.4g}{22}$×2×9=3.6g,根据质量守恒定律得Y质量=4.4g+3.6g-1.6g=6.4g,此反应中Y和M的质量比=6.4g:3.6g=16:9,
故答案为:3.6g;16:9;质量守恒定律.
点评 本题考查化学方程式有关计算,明确各个物理量关系是解本题关键,侧重考查学生分析计算能力,易错点是M质量的计算,题目难度不大.

练习册系列答案
相关题目
18.常温下某溶液中只含有Na+、H+、OH-、A-四种离子,下列说法正确的是( )
| A. | 若溶质为NaA,溶液中可能存在:c (OH-)=c(H+)+c(HA) | |
| B. | 若c(OH-)>c(H+),溶液中不可能存在c(Na+)>c(OH-)>c(A-)>c(H+) | |
| C. | 溶液中可能存在c(Na+)>c(A-)>c(H+)>c(OH-) | |
| D. | 若溶质为NaA和HA,则一定存在c(A-)>c(Na+)>c(H+)>c(OH-) |
19.硼有两种天然同位素105B和115B,已知硼元素的原子量为10.8.下列对硼元素中115B的质量分数的判断正确的是( )
| A. | 等于80% | B. | 略小于80% | C. | 略大于80% | D. | 等于20% |
16.有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同.下列事实能说明上述观点的是( )
| A. | 乙酸易溶于水,而乙烷难溶于水 | |
| B. | 乙烯能发生加成反应,乙烷不能发生加成反应 | |
| C. | 甲苯能使高锰酸钾溶液褪色,甲烷和苯不能使高锰酸钾溶液褪色 | |
| D. | 乙醛与Ag(NH3)2 OH 1:2 反应.而甲醛为 1:4 |
3.萤火虫的发光是荧光素在催化作用下发生复杂的生化反应并释放光能,其原理可以简单表示如下:

关于荧光素及氧化荧光素的叙述,正确的是( )

关于荧光素及氧化荧光素的叙述,正确的是( )
| A. | 互为同系物 | B. | 均可发生硝化反应 | ||
| C. | 均可与碳酸氢钠反应 | D. | 均最多有7个碳原子共平面 |
16. 某研究性学习小组对铝热反应实验展开研究.现行高中化学教材中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
某研究性学习小组对铝热反应实验展开研究.现行高中化学教材中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
Ⅰ.(1)某同学推测,铝热反应所得到的熔融物应是铁铝合金.理由是:该反应放出的热量使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金.你认为他的解释是否合理?答:合理(填“合理”或“不合理”)
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝.该实验所用试剂是NaOH溶液
反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
(3)实验室溶解该熔融物,下列试剂中最好的是B (填序号).
A.浓硫酸 B.稀硫酸 C.稀硝酸 D.氢氧化钠溶液
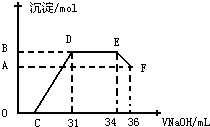
Ⅱ.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol•L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.试回答下列问题:
(1)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为H++OH-=H2O
(2)在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为NH4++OH-=NH3•H2O
上述现象说明溶液中Al3+、Fe3+、H+结合OH-的能力比NH4+强(填离子符号).
(3)B点对应的沉淀的物质的量为0.032molmol,C点对应的氢氧化钠溶液的体积为7mL.
 某研究性学习小组对铝热反应实验展开研究.现行高中化学教材中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
某研究性学习小组对铝热反应实验展开研究.现行高中化学教材中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | -- |
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝.该实验所用试剂是NaOH溶液
反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
(3)实验室溶解该熔融物,下列试剂中最好的是B (填序号).
A.浓硫酸 B.稀硫酸 C.稀硝酸 D.氢氧化钠溶液
Ⅱ.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol•L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.试回答下列问题:
(1)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为H++OH-=H2O
(2)在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为NH4++OH-=NH3•H2O
上述现象说明溶液中Al3+、Fe3+、H+结合OH-的能力比NH4+强(填离子符号).
(3)B点对应的沉淀的物质的量为0.032molmol,C点对应的氢氧化钠溶液的体积为7mL.