题目内容
化学已渗透到人类生活的各个方面.下列说法错误的是( )
| A、阿司匹林具有解热镇痛作用 |
| B、可以用Si3N4、Al2O3制作高温结构陶瓷制品 |
| C、禁止使用四乙基铅作汽油抗爆震剂,可减少汽车尾气污染 |
| D、在入海口的钢铁闸门上装一定数量的铜块可防止闸门被腐蚀 |
考点:药物的主要成分和疗效,金属的电化学腐蚀与防护,常见的生活环境的污染及治理
专题:化学应用
分析:A.阿司匹林是生活中的常用解热镇痛药物;
B.制作高温结构陶瓷制品的原料的熔点应较高;
C.铅能使人体中毒;
D.原电池能加快化学反应速率.
B.制作高温结构陶瓷制品的原料的熔点应较高;
C.铅能使人体中毒;
D.原电池能加快化学反应速率.
解答:
解:A.阿司匹林是生活中的常用解热镇痛药物,一般用来治疗感冒发烧,故A正确;
B.制作高温结构陶瓷制品的原料的熔点应较高,氮化硅陶瓷、三氧化二铝的熔点很高,故B正确;
C.因铅能使人体中毒,则禁止使用四乙基铅作汽油防爆剂来减少铅污染,故C正确;
D.因铁铜相比,铁更活泼,由原电池原理可知铁更易发生氧化发应而损耗,故D错误.
故选D.
B.制作高温结构陶瓷制品的原料的熔点应较高,氮化硅陶瓷、三氧化二铝的熔点很高,故B正确;
C.因铅能使人体中毒,则禁止使用四乙基铅作汽油防爆剂来减少铅污染,故C正确;
D.因铁铜相比,铁更活泼,由原电池原理可知铁更易发生氧化发应而损耗,故D错误.
故选D.
点评:本题考查了化学与社会、科学、生活、环境等问题,难度不大,此考点属于学习化学的基本素养,也是高考化学试题的热点问题,这一考点往往为常识性的知识与运用化学原理解决实际问题,应予以重视.

练习册系列答案
相关题目
下列实验装置与描述正确的是( )
A、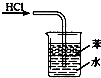 用于吸收HCl气体 |
B、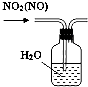 用于除去NO2中的NO |
C、 配制1mol/L NaCl溶液定容操作 |
D、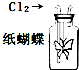 滴有淀粉碘化钾溶液的纸蝴蝶变蓝 |
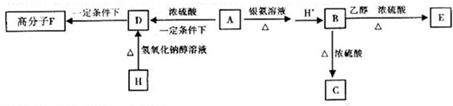
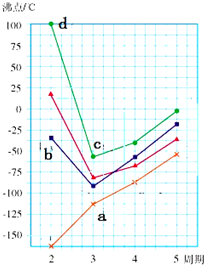 A、B、D、E、F、G是原子序数依次增大的六种短周期元素.A和B能形成B2A和B2A2两种化合物,B、D、G的最高价氧化物对应水化物两两之间都能反应,D、F、G原子最外层电子数之和等于15.
A、B、D、E、F、G是原子序数依次增大的六种短周期元素.A和B能形成B2A和B2A2两种化合物,B、D、G的最高价氧化物对应水化物两两之间都能反应,D、F、G原子最外层电子数之和等于15.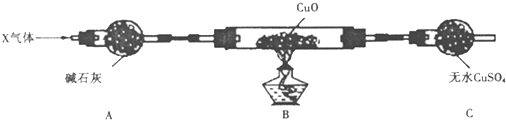
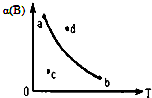 条件一定时,反应2A(g)+B(g)?2C(g),B的转化率α与温度T变化关系曲线图如图所示,图中4个点中,表示未达到平衡状态,且V正<V逆的点是( )
条件一定时,反应2A(g)+B(g)?2C(g),B的转化率α与温度T变化关系曲线图如图所示,图中4个点中,表示未达到平衡状态,且V正<V逆的点是( )