题目内容
18.按以下装置图进行实验,填写有关现象及化学方程式.
(1)B中浓硫酸的作用是干燥气体;
(2)C中发生反应的化学方程式为2Na2O2+2CO2═2Na2CO3+O2↑;
(3)D中现象是澄清石灰水变浑浊,反应的离子方程式是CO2+Ca2++2OH-═CaCO3↓+H2O;
(4)E中收集的气体是O2.
分析 实验考查二氧化碳与过氧化钠的反应,A装置加热碳酸氢钠使其分解生成二氧化碳和水,碳酸钠,二氧化碳和水经过盛有浓硫酸的洗气瓶除去二氧化碳中的水,剩余二氧化碳与C装置过氧化钠反应生成碳酸钠和氧气,从C处出来的气体为二氧化碳和氧气的混合气体,通过盛有澄清石灰水的D装置,二氧化碳与氢氧化钙反应生成碳酸钙沉淀,被澄清石灰水吸水,剩余氧气用排水法收集;
(1)碳酸氢钠受热分解生成碳酸钠和水、二氧化碳;浓硫酸具有吸水性,能够干燥二氧化碳;
(2)二氧化碳与过氧化钠反应生成碳酸钠和氧气;
(3)二氧化碳与氢氧化钙反应生成碳酸钙和水;
(4)二氧化碳与过氧化钠反应生成碳酸钠和氧气,从C中出来的气体为二氧化碳和氧气的混合气体,通过澄清石灰水,能够将二氧化碳稀吸收,剩余气体为氧气;
解答 解:(1)A中分解碳酸氢钠生成二氧化碳、和水,通过盛有浓硫酸的B可以除去二氧化碳中的水蒸气;
故答案为:干燥气体(吸收水分);
(2)二氧化碳与过氧化钠反应生成碳酸钠和氧气,方程式:2Na2O2+2CO2═2Na2CO3+O2↑;
故答案为:2Na2O2+2CO2═2Na2CO3+O2↑;
(3)二氧化碳与氢氧化钙反应生成碳酸钙和水,所以看到现象为;澄清石灰水变浑浊,反应的离子方程式:CO2+Ca2++2OH-═CaCO3↓+H2O
;
故答案为:澄清石灰水变浑浊,CO2+Ca2++2OH-═CaCO3↓+H2O;
(4)二氧化碳与过氧化钠反应生成碳酸钠和氧气,从C中出来的气体为二氧化碳和氧气的混合气体,通过澄清石灰水,能够将二氧化碳稀吸收,剩余气体为氧气,所以E中收集的气体为氧气,化学式:O2;
故答案为:O2;
点评 本题考察过氧化钠与二氧化碳反应,明确碳酸氢钠、过氧化钠的性质是解题关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.下列有机物中,能发生消去反应生成2种烯烃,又能发生水解反应的是( )
| A. | 1-溴丁烷 | B. | 2-甲基-3-氯戊烷 | ||
| C. | 2,2-二甲基-1-氯丁烷 | D. | 一氯甲烷 |
9.V、W、X、Y均是元素周期表中短周期元素,在周期表中的相对位置关系如表所示:
V的最简单氢化物为甲,W的最简单氢化物为乙,甲、乙混合时有白烟生成.下列说法正确的是( )
| Y | V | |||
| X | W |
| A. | 原子半径:X>W>V>Y | |
| B. | Y的最高价氧化物的电子式为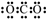 | |
| C. | X的最高价氧化物能与V、W最高价氧化物对应的水化物反应 | |
| D. | 甲、乙混合时所生成的物质为离子化合物,既含有离子键又含有非极性键 |
6.下列反应前后物质的总能量变化能用右图表示的是( )
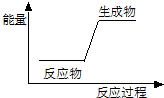

| A. | 生石灰和水的反应 | B. | 木炭在氧气中燃烧 | ||
| C. | 石灰石在高温下的分解反应 | D. | 盐酸与氢氧化钠溶液的反应 |
13.A、B、C、D、E、F是中学化学中常见的六种短周期元素,有关位置及信息如下:A的气态氢化物能使湿润的红色石蕊试纸变蓝;C单质在实验室一般保存在煤油中;F的最高价氧化物对应的水化物既能与酸反应又能与碱反应,G单质是日常生活中用量最大的金属,易被腐蚀.请回答下列问题:
(1)G元素在周期表中的位置是第四周期第Ⅷ族.
(2)A与B可组成质量比为7:16的三原子分子,该分子与水反应的化学方程式:3NO2+H2O=2HNO3+NO;
(3)同温同压下,将a L A氢化物的气体和b L D的氢化物气体通入水中,若a=b,则所得溶液的pH<7(填“>“或“<”或“=”),若所得溶液的pH=7,则a>b(填“>“或“<”或“=”)
(4)写出F的单质与NaOH溶液反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
(5)已知一定量的E单质能在B2(g)中燃烧,其可能的产物及能量关系如图1所示:请写出一定条件下EB2(g)与E(s)反应生成EB(g)的热化学方程式CO2(g)+C(s)=2CO(g)△H=+172.5kJ/mol.
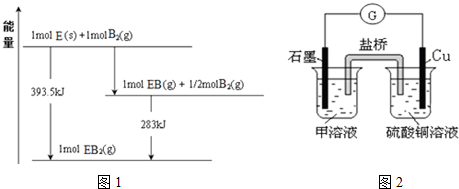
(6)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图2所示,其反应中正极反应式为Fe3++e-=Fe2+.
| … | E | A | B | ||
| C | … | D |
(2)A与B可组成质量比为7:16的三原子分子,该分子与水反应的化学方程式:3NO2+H2O=2HNO3+NO;
(3)同温同压下,将a L A氢化物的气体和b L D的氢化物气体通入水中,若a=b,则所得溶液的pH<7(填“>“或“<”或“=”),若所得溶液的pH=7,则a>b(填“>“或“<”或“=”)
(4)写出F的单质与NaOH溶液反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
(5)已知一定量的E单质能在B2(g)中燃烧,其可能的产物及能量关系如图1所示:请写出一定条件下EB2(g)与E(s)反应生成EB(g)的热化学方程式CO2(g)+C(s)=2CO(g)△H=+172.5kJ/mol.

(6)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图2所示,其反应中正极反应式为Fe3++e-=Fe2+.
10.下列有关实验操作、现象和结论正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将某气体通入FeCl2溶液中 | 溶液由浅绿色变为黄色 | 该气体中一定含有Cl2 |
| B | 将某气体通入品红溶液中 | 品红溶液褪色 | 该气体中一定含有SO2 |
| C | 将某气体通过灼热的CuO粉末 | 粉末由黑变红 | 该气体中一定含有H2 |
| D | 将某气体与湿润的红色石蕊试纸接触 | 试纸变蓝色 | 该气体中一定含有NH3 |
| A. | A | B. | B | C. | C | D. | D |
7.在下列物质中,能够导电的电解质是( )
| A. | 食盐晶体 | B. | 无水乙醇 | C. | 熔融的氯化钾 | D. | 稀硫酸溶液 |
8.对于有气体参加的化学反应来说,下列说法不正确的是( )
| A. | 压缩容器体积,增大压强,活化分子百分数不变,化学反应速率增大 | |
| B. | 升高温度,活化分子百分数增大,化学反应速率增大 | |
| C. | 加入反应物,活化分子百分数增大,化学反应速率增大 | |
| D. | 使用催化剂,降低了反应所需的活化能,活化分子百分数增大,化学反应速率增大 |