题目内容
9.(1)常温下.某强酸溶液pH=a,某强碱溶液pH=b,已知a+b=12,酸碱溶液混合后pH=7,则酸溶液体积V(酸)和碱溶液体积V(碱)的正确关系V(碱)=102 V(酸)(2)取浓度相同的NaOH和HCl溶液,以3:2体积比相混合,所得溶液的pH 等于12,则原溶液的浓度为0.05 mol/L
(3)纯水中c(H+)=5×10-7mol/L,则此时纯水中的c(OH-)=5.0×10-7mol/L;
若温度不变,滴入稀硫酸使c(H+)=5.0×10-3mol/L,则c(OH-)=5.0×10-11mol/L;
在该温度时,往水中滴入NaOH溶液,溶液中的C(OH-)=5.0×10-2 mol/L,则溶液中c(H+)=5.0×10-12mol/L.
分析 (1)25℃时,Kw=10-14,某强酸溶液pH=a,则该酸溶液中氢离子浓度为10-a mol/L,强碱溶液pH=b,则碱溶液中氢氧根离子浓度=10 b-14 mol/L,混合后溶液的pH=7说明氢离子和氢氧根离子的物质的量相等,据此解答;
(2)酸碱混合后,pH=12,则碱过量,剩余的c(OH-)=0.01mol/L,以此来计算;
(3)根据纯水中c(OH-)=c(H+),溶液显示中性进行分析;根据该温度下纯水中氢离子浓度和氢氧根离子浓度,计算出水的离子积;若温度不变,根据稀硫酸溶液中氢离子浓度和水的离子积计算出溶液中氢氧根离子的浓度;若温度不变,依据氢氧化钠溶液中氢氧根离子浓度,结合离子积常数计算溶液中氢离子浓度.
解答 解:(1)25℃时,Kw=10-14,某强酸溶液pH=a,则该酸溶液中氢离子浓度为10-a mol/L,强碱溶液pH=b,则碱溶液中氢氧根离子浓度=10 b-14 mol/L,混合后溶液的pH=7说明氢离子和氢氧根离子的物质的量相等,设酸的体积为V(酸),碱的体积为V(碱),10-a mol/L×V(酸)L=10 b-14 mol/L×V(碱)L,则V(酸)=10 a+b-14 V(碱),而a+b=12,故V(碱)=102 V(酸);
故答案为:V(碱)=102 V(酸);
(2)设NaOH和HCl的物质的量浓度均为x,NaOH和HCl溶液以3:2体积比相混合,体积分别为3V、2V,
酸碱混合后,pH=12,则碱过量,剩余的c(OH-)=0.01mol/L,
则$\frac{3V×x-2V×x}{5V}$=0.01mol/L,
解得x=0.05mol/L;
故答案为:0.05 mol/L;
(3)纯水显示中性,c(OH-)=c(H+)=5.0×10-7mol/L;此温度下,水的离子积为:Kw=5.0×10-7×5.0×10-7=2.5×10-13,若温度不变,滴入稀硫酸使c(H+)=5.0×10-3mol/L,硫酸溶液中氢离子浓度c(H+)=5.0×10-3mol/L,c(OH-)=$\frac{2.5×1{0}^{-13}}{5.0×1{0}^{-3}}$mol/L=5.0×10-11 mol/L,
在该温度时,往水中滴入NaOH溶液,溶液中的c(OH-)=5.0×10-2mol/L,则溶液中c(H+)=$\frac{2.5×1{0}^{-13}}{5.0×1{0}^{-6}}$mol/L=5×10-12mol/L,
故答案为:5.0×10-7mol/L;5.0×10-11mol/L;5×10-12mol/L.
点评 本题考查了离子积常数的有关计算,题目难度中等,根据溶液的酸碱性及水的离子积常数来分析解答,注意该温度下纯水中c(H+)=5×10-7mol/L,则水的离子积常数是2.50-13,为易错点.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | Cu+4HNO3═Cu(NO3)2+2NO2↑+2H2O | B. | 2NaOH+CuSO4═Na2SO4+Cu(OH)2↓ | ||
| C. | 2CO+O2═2CO2 | D. | 2Al+2NaOH+2H2O═2NaAlO2+3H2↑ |

| A. | 第Ⅱ步的离子方程式为Na++NH3+H2O+CO2→NaHCO3↓+NH4+ | |
| B. | 第Ⅲ步得到的晶体是Na2CO3•10H2O | |
| C. | A气体是CO2,B气体是NH3 | |
| D. | 第Ⅳ步操作的过程主要有溶解、蒸发、结晶 |
(2)在用Na2SO3溶液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如下表:
| n(SO32-):n(HSO3-) | 1:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
(3)向0.1mol•L-1的NaHSO3中通人氨气至溶液呈中性时,溶液中的c(H+)、c(OH-)、c(SO32-)、c(Na+)、c(NH4+)这五种离子浓度大小关系是c(Na+)>c(SO32-)>c(NH4+)>c(H+)=c(OH-).
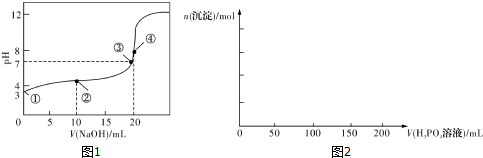
(4)已知Ca3(PO4)2、CaHPO4均难溶于水,而Ca(H2PO4)2易溶,在含0.1molCa(OH)2的澄清石灰水中逐滴加人1mol•L-1的H3PO4:请在图2中作出生成沉淀的物质的量随H3PO4滴人体积从0开始至200mL的图象.
Ⅰ.甲化学兴趣小组取20.00mL待测稀盐酸放入锥形瓶中,并滴加2~3滴酚酞溶液作指示剂,用0.2000mol•L-1的标准NaOH溶液进行滴定.重复上述滴定操作3次,并记录数据.
(1)滴定时边滴边摇动锥形瓶,眼睛应观察B.(填序号)
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
(2)判断滴定终点的现象是:溶液从无色变为浅红色,且半分钟内不变色.
(3)根据下列数据:请计算待测盐酸溶液的浓度为0.2000mol/L.
| 滴定次数 | 待测液体积(mL) | 标准NaOH溶液读数记录(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.40 | 20.40 |
| 第二次 | 20.00 | 4.00 | 24.00 |
| 第三次 | 20.00 | 2.00 | 24.10 |
①取水样10.0ml于锥形瓶中,加入10.0ml的KI溶液(足量),滴入指示剂2~3滴.
②将自己配制的0.01mol•L-1标准Na2S2O3溶液装入滴定管中,调整液面,记下读数.
③将锥形瓶置于滴定管下进行滴定,发生的反应为:I2+2Na2S2O3=2NaI+2Na2S4O6.试回答下列问答:
(1)步骤①发生的化学反应方程式为:Cl2+KI=I2+2KCl;加入的指示剂是淀粉溶液.
(2)步骤②应使用碱式滴定管.
(3)氯的所测浓度比实际浓度会偏大,造成误差的原因可能是ACE(填序号)
A 配制标准Na2S2O3溶液定容时,加水超过刻度线
B 锥形瓶水洗后直接装待测水样
C 装标准Na2S2O3溶液的滴定管水洗后没有润洗
D 滴定到达终点时,俯视读出滴定管读数;
E 滴定前尖嘴部分有气泡,滴定后消失
Ⅲ.沉淀滴定所用的指示剂本身就是一种沉淀剂.已知一些银盐的颜色和Ksp(20℃)如下表,测定水体中氯化物的含量,常用标准硝酸银溶液进行滴定.
| 化学式 | AgCl | AgBr | AgI | Ag2S | Ag2CrO4 |
| 颜色 | 白色 | 浅黄色 | 黄色 | 黑色 | 红色 |
| Ksp | 2.0×10-10 | 5.4×10-13 | 8.3×10-17 | 2.0×10-48 | 2.0×10-12 |
A.KBrB.KIC.K2S D.K2CrO4
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,$\frac{c(Br-)}{c(Cl-)}$=2.7×10-3.
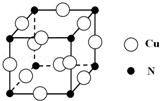 硼和氮元素在化学中有很重要的地位,回答下列问题:
硼和氮元素在化学中有很重要的地位,回答下列问题: .预计于2017年发射的“嫦娥五号”探测器采用的长征5号运载火箭燃料为偏二甲肼[(CH3)2NNH2].(CH3)2NNH2中N原子的杂化方式为sp3.
.预计于2017年发射的“嫦娥五号”探测器采用的长征5号运载火箭燃料为偏二甲肼[(CH3)2NNH2].(CH3)2NNH2中N原子的杂化方式为sp3.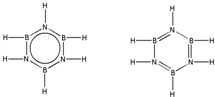 .
.