题目内容
9.常温下,向10mL0.1mol•L-1的HR溶液中0.1mol•L-1的氨水,下列分析不正确的是( )| A. | 开始滴加氨水后溶液导电能力逐渐增强,说明HR为弱酸 | |
| B. | 滴入10mL氨水后酸碱恰好中和,此时溶液pH=7 | |
| C. | 随若氨水的加入,当c(OH-)>c(H+)时,c(NH4+)>(R-) | |
| D. | 该过程中溶液均有c(H+)•c(OH-)=KW=1.0×10-14 |
分析 A、向10mL0.1mol•L-1的HR溶液中0.1mol•L-1的氨水,生成铵盐溶液中自由移动离子的浓度增加;
B、滴入10mL氨水后酸碱恰好中和,此时溶液pH不一定为7,与HR与氨水的电离度相对大小有关;
C、根据电荷守恒分析解答;
D、常温下任何稀的电解质溶液中存在c(H+)•c(OH-)=KW=1.0×10-14.
解答 解:A、向10mL0.1mol•L-1的HR溶液中0.1mol•L-1的氨水,生成铵盐溶液中自由移动离子的浓度增加,所以导电能力增加,故A正确;
B、滴入10mL氨水后酸碱恰好中和,此时溶液pH不一定为7,与HR与氨水的电离度相对大小有关,如果HR的电离度与氨水的电离度相等,则此溶液呈中性,故B错误;
C、根据电荷守恒得:c(OH-)+(R-)=c(H+)+c(NH4+),如果c(OH-)>c(H+),则c(NH4+)>(R-),故C正确;
D、常温下任何稀的电解质溶液中存在c(H+)•c(OH-)=KW=1.0×10-14,故D正确;
故选B.
点评 本题考查了酸碱混合的定性判断、离子浓度定性比较、溶液导电性及其影响等知识,题目难度中等,明确酸碱混合的定性判断及溶液酸碱性与溶液pH的计算方法为解答关键,试题侧重考查学生的分析、理解能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.滴定分析中,测定结果的相对误差一般在 左右.( )
| A. | 2×10-3 | B. | 2×10-2 | C. | 2×10-1 | D. | 2×10-4 |
17.某溶液X含有K+、Mg2+、Fe3+、Al3+、Fe2+、Cl-、CO32-、OH-、SiO32-、NO3-、SO42-中的几种,已知该溶液中各离子物质的量浓度均为0.2mol•L-1(不考虑水的电离及离子的水解).为确定该溶液中含有的离子,现进行了如下的操作:
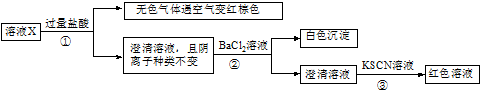
下列说法正确的是( )

下列说法正确的是( )
| A. | 无色气体可能是NO和CO2的混合物 | |
| B. | 原溶液可能存在Fe3+ | |
| C. | 溶液X中所含离子种类共有4种 | |
| D. | 另取l00mL原溶液X,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,理论上得到的固体质量为2.4g |
4.在短周期元素中,X元素与Y、Z、W三元素相邻,X、Y的原子序数之和等于Z的原子序数,这四种元素原子的最外层电子数之和为20.下列判断正确的是( )
| A. | 四种元素均可与氢元素形成 18电子分子 | |
| B. | X、Y、Z、W形成的单质最多有 6种 | |
| C. | 四种元素中,Z的最高价氧化物对应水化物酸性最强 | |
| D. | 四种元素的原子半径:rZ>rX>rY>rW |
18.W、X、Y、Z均为短周期主族元素,原子序数依次增大.W的最外层电子数、电子层数和主族序数均相等.Y原子最外层电子数与W、X原子最外层电子数之和相等.X原子的最外层电子数是内层电子数的2倍还多1个.Z是所在周期中主族元素原子半径最大的元素.下列说法正确的是( )
| A. | 离子半径大小顺序为:Z>X>Y>W | |
| B. | W、X、Y三种元素都属于非金属元素,它们之间只能形成共价化合物 | |
| C. | X、Y、Z三种元素与W 元素形成的最简单化合物的沸点依次升高 | |
| D. | X、Y、Z三种元素形成的化合物的水溶液一定显中性 |
19.根据等电子原理,下列各组分子或离子的空间构型不相似的是( )
| A. | NH4+和CH4 | B. | H3O+和NH3 | C. | NO3-和CO32- | D. | CO2和H2O |
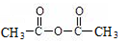 +H-OH→2
+H-OH→2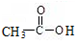
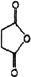 .
.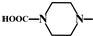 外,还需含苯环的二羟基化合物F,写如有机物F与NaOH溶液反应的离子反应方程式
外,还需含苯环的二羟基化合物F,写如有机物F与NaOH溶液反应的离子反应方程式 ,有机物G是F的同分异构体,有机物G遇FeCl3溶液显紫色,且有4种不同类型的氢,其个数比为3:2:2:1,则符合条件的有机物G的同分异构体有3种.写出其中一种的结构简式
,有机物G是F的同分异构体,有机物G遇FeCl3溶液显紫色,且有4种不同类型的氢,其个数比为3:2:2:1,则符合条件的有机物G的同分异构体有3种.写出其中一种的结构简式 或
或 或
或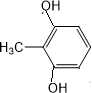 .
.