题目内容
 A、B、D、E、W是元素周期表前四周期中常见的元素,其相关信息如下表:
A、B、D、E、W是元素周期表前四周期中常见的元素,其相关信息如下表:| 元素 | 相关信息 |
| A | A原子L层电子数是K层电子数的2倍 |
| B | B是地壳中含量最多的元素 |
| D | 在第3周期元素中,它的简单离子半径最小 |
| E | E存在质量数为23,中子数为12的核素 |
| W | W有多种化合价,其白色氢氧化合物在空气中会迅速变成灰绿色,最后变成红褐色 |
(2)A 和B的气态氢化物中,较稳定的是
(3)写出W的白色氢氧化合物在空气中会迅速变成灰绿色,最后变成红褐色这个过程的化学方程式:
(4)写出D和B组成的二元化合物与E的最高价氧化物的水化物反应的离子方程式:
(5)将一定质量的Mg和D的混合物投入500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则固体混合物中D的质量为
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A的原子L层电子数是K层电子数的2倍,则A为C元素;B是地壳中含量最多的元素,则B为O元素;D在第3周期元素中,它的简单离子半径最小,则D为Al元素;E存在质量数为23,中子数为12的核素,则其质子数为:23-12=11,则Z为Na;W有多种化合价,其白色氢氧化合物在空气中会迅速变成灰绿色,最后变成红褐色,则W为Fe,据此进行解答.
解答:
解:A的原子L层电子数是K层电子数的2倍,则A为C元素;B是地壳中含量最多的元素,则B为O元素;D在第3周期元素中,它的简单离子半径最小,则D为Al元素;E存在质量数为23,中子数为12的核素,则其质子数为:23-12=11,则Z为Na;W有多种化合价,其白色氢氧化合物在空气中会迅速变成灰绿色,最后变成红褐色,则W为Fe,
(1)W为Fe,原子序数为26,位于元素周期表第四周期第Ⅷ族,
故答案为:第四周期第Ⅷ族;
(2)A为C、B为O元素,非金属性:O>C,则C元素和O元素的气态氢化物中较稳定的是H2O;E2B2为过氧化钠,属于离子化合物,其电子式为: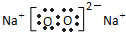 ,
,
故答案为:H2O;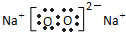 ;
;
(3)W的白色氢氧化合物在空气中会迅速变成灰绿色,最后变成红褐色这个过程的化学方程式为:4Fe(OH)2+O2+2H2O═4Fe(OH)3,
故答案为:4Fe(OH)2+O2+2H2O═4Fe(OH)3;
(4)D和B组成的二元化合物为Al2O3,Al2O3与E的最高价氧化物的水化物NaOH反应的离子方程式为:Al2O3+2OH-═2AlO2-+H2O,
故答案为:Al2O3+2OH-═2AlO2-+H2O;
(5)根据图象可知,生成氢氧化铝沉淀的物质的量为:0.35mol-0.15mol=0.2mol,根据质量守恒定律可知Al的质量为:27g/mol×0.2mol=5.4g;
溶解0.2mol氢氧化铝消耗氢氧化钠的物质的量为0.2mol,氢氧化钠溶液的体积为:240mL-200mL=40mL,则该氢氧化钠溶液的浓度为:
=5mol/L,
当加入200mL氢氧化钠溶液是,沉淀的物质的量达到最大,此时溶质为硫酸钠,则消耗硫酸的物质的量为:
=0.5mol,所以该硫酸的浓度为:
=1mol/L,
故答案为:5.4g;1mol?L-1.
(1)W为Fe,原子序数为26,位于元素周期表第四周期第Ⅷ族,
故答案为:第四周期第Ⅷ族;
(2)A为C、B为O元素,非金属性:O>C,则C元素和O元素的气态氢化物中较稳定的是H2O;E2B2为过氧化钠,属于离子化合物,其电子式为:
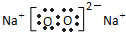 ,
,故答案为:H2O;
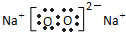 ;
;(3)W的白色氢氧化合物在空气中会迅速变成灰绿色,最后变成红褐色这个过程的化学方程式为:4Fe(OH)2+O2+2H2O═4Fe(OH)3,
故答案为:4Fe(OH)2+O2+2H2O═4Fe(OH)3;
(4)D和B组成的二元化合物为Al2O3,Al2O3与E的最高价氧化物的水化物NaOH反应的离子方程式为:Al2O3+2OH-═2AlO2-+H2O,
故答案为:Al2O3+2OH-═2AlO2-+H2O;
(5)根据图象可知,生成氢氧化铝沉淀的物质的量为:0.35mol-0.15mol=0.2mol,根据质量守恒定律可知Al的质量为:27g/mol×0.2mol=5.4g;
溶解0.2mol氢氧化铝消耗氢氧化钠的物质的量为0.2mol,氢氧化钠溶液的体积为:240mL-200mL=40mL,则该氢氧化钠溶液的浓度为:
| 0.2mol |
| 0.04L |
当加入200mL氢氧化钠溶液是,沉淀的物质的量达到最大,此时溶质为硫酸钠,则消耗硫酸的物质的量为:
| 5mol/L×0.2L |
| 2 |
| 0.5mol |
| 0.5L |
故答案为:5.4g;1mol?L-1.
点评:本题考查了位置、结构与性质的关系,题目难度中等,正确推断各元素名称为解答关键,注意掌握元素周期表结构、元素周期律内容,(5)为难点,需要明确图象中曲线变化的含义.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
向27.2gCu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO 和Cu(NO3)2.在所得溶液中加入1.0mol/L 的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,经洗涤、干燥,沉淀的质量为39.2g.下列有关说法不正确的是( )
| A、原混合物中含氧原子的质量为1.6g |
| B、硝酸的物质的量浓度为2.4mol/L |
| C、反应中产生NO的体积为4.48L |
| D、固体物质溶解后剩余HNO3为0.2mol |
有NaCl、NH4Cl、AlCl3、CuCl2、Na2SO4五种溶液,只用一种试剂把它们鉴别开来,该试剂是( )
| A、盐酸 | B、烧碱溶液 |
| C、氯化钡溶液 | D、氢氧化钡溶液 |
下列各组中的两种物质作用,反应条件(温度或者反应物用量)改变,不会引起产物种类改变的是( )
| A、Na和O2 |
| B、Na2O2和H2O |
| C、NaOH和CO2 |
| D、Na2CO3和HCl |
某基态原子的N能层上有2个电子,他对应的二价阳离子所含质子数不可能为( )
| A、22 | B、25 | C、26 | D、29 |




 A、B、C、D四种短周期元素,A、B、C同周期,A的原子半径是同周期中最大的;B、D同主族.已知D原子最外层电子数是电子层数的3倍,C元素的单质可以从A、B两元素组成的化合物的水溶液中置换出B元素的单质.
A、B、C、D四种短周期元素,A、B、C同周期,A的原子半径是同周期中最大的;B、D同主族.已知D原子最外层电子数是电子层数的3倍,C元素的单质可以从A、B两元素组成的化合物的水溶液中置换出B元素的单质.