题目内容
某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变成H2、CO.其过程如下:下列说法不正确的是( )


| A、该过程中CeO2没有消耗 |
| B、如图中△H1=-(△H2+△H3) |
| C、该过程实现了太阳能向化学能的转化 |
| D、加入催化剂反应的焓变减小 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、总反应为:H2O+CO2→H2+CO+O2,CeO2没有消耗,是催化剂;
B、根据盖斯定律,△H1=-(△H2+△H3);
C、该过程中在太阳能作用下将H2O、CO2转变为H2、CO;
D、加入催化剂改变反应速率不改变化学平衡.
B、根据盖斯定律,△H1=-(△H2+△H3);
C、该过程中在太阳能作用下将H2O、CO2转变为H2、CO;
D、加入催化剂改变反应速率不改变化学平衡.
解答:
解:A、通过太阳能实现总反应:H2O+CO2→H2+CO+O2,CeO2没有消耗,CeO2是光催化剂,故A正确;
B、由图可知,根据盖斯定律,应该是:△H1=-(△H2+△H3),故B正确;
C、该过程中在太阳能作用下将H2O、CO2转变为H2、CO,所以把太阳能转变成化学能,故C正确;
D、加入催化剂改变反应速率不改变化学平衡,反应焓变不变,故D错误;
故选D.
B、由图可知,根据盖斯定律,应该是:△H1=-(△H2+△H3),故B正确;
C、该过程中在太阳能作用下将H2O、CO2转变为H2、CO,所以把太阳能转变成化学能,故C正确;
D、加入催化剂改变反应速率不改变化学平衡,反应焓变不变,故D错误;
故选D.
点评:本题考查了热化学知识和盖斯定律的应用,以及催化剂的判断,能量变化形式的判断,题目难度适中.

练习册系列答案
相关题目
下列物质可以用铝制容器存放的( )
| A、浓硝酸 | B、稀硝酸 |
| C、浓盐酸 | D、浓氢氧化钠溶液 |
现在探索、开发的新能源有( )
①核能 ②柴草 ③煤炭 ④太阳能 ⑤氢能 ⑥液化石油气⑦水煤气 ⑧天然气.
①核能 ②柴草 ③煤炭 ④太阳能 ⑤氢能 ⑥液化石油气⑦水煤气 ⑧天然气.
| A、①④⑤ | B、②③⑥⑦ |
| C、③⑥⑦⑧ | D、①②④ |
已知硫酸亚铁溶液中加入过氧化钠时发生反应:4Fe2++4Na2O2+6H2O═4Fe(OH)3↓+O2↑+8Na+,则下列说法正确的是( )
| A、该反应中还原剂为Fe2+,O2、Fe(OH)3均为氧化产物 |
| B、若有4molNa2O2参加反应,则反应中共得到8NA个电子 |
| C、标准状况下,每生成22.4LO2,则有4molNa2O2被还原 |
| D、反应过程中可以看到白色沉淀转化为灰绿色再转化为红褐色沉淀 |
下列关于粒子结构的描述不正确的是( )
| A、H2S和NH3均是价电子总数为8的极性分子 |
| B、HS-和HCl均是含一个极性键的18电子粒子 |
| C、1molD216O中含中子、质子、电子各10NA(NA代表阿伏加德罗常数的值) |
| D、CH2C12和CCl4均是四面体构型的非极性分子 |
下列有关化学用语错误的是( )
A、乙醇分子球棍模型: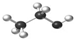 | ||
B、8个中子的碳原子的核素符号:
| ||
C、-OH的电子式: | ||
D、CH4Si的结构式: |
下列单体能在一定条件下加聚反应生成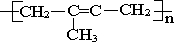 的是( )
的是( )
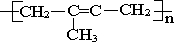 的是( )
的是( )| A、丙烯 |
| B、2-甲基-1,3-丁二烯 |
| C、乙烯和丙烯 |
| D、2-甲基-2-丁烯 |
