��Ŀ����
 X��Y��Z��M��Q��R��6�ֶ�����Ԫ�أ���ԭ�Ӱ뾶����Ҫ���ϼ����£�
X��Y��Z��M��Q��R��6�ֶ�����Ԫ�أ���ԭ�Ӱ뾶����Ҫ���ϼ����£�| Ԫ�ش��� | X | Y | Z | M | Q | R |
| ԭ�Ӱ뾶/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 | 0.037 |
| ��Ҫ���ϼ� | +2 | +3 | +6��-2 | +2 | -2 | +1 |
��2��X��Y��Q�����γɼ����ӣ��������Ӱ뾶������
��3�����ڱ�����Щ���ڶԽǣ����ϡ����£�λ�õ�Ԫ�أ����ǵĵ��ʼ��仯��������ʴ��ڡ��Խ������ơ���������M����������ǿ����Һ��Ӧ�����ӷ���ʽ��
��4��Q��R��ԭ�Ӹ�����1��1��ɵĻ�����ף���һ�֡���ɫ����������
�ټ����������ۼ�������
�ڿ�������������Ʊ���װ����ͼ��ʾ���ڼ�����Һ�У�����
�����е�������ԭ�õ���ϡ�����Һ��ͼ��ֱ����Դ��a��
���㣺λ�ýṹ���ʵ����ϵӦ��
ר�⣺Ԫ����������Ԫ�����ڱ�ר��
������X��M�Ļ��ϼ۶�Ϊ+2�ۣ�ӦΪ���ڱ��ڢ�A�壬���ݰ뾶��ϵ��֪MΪBe��XΪMg��Z��Q�Ļ��ϼ۶���-2�ۣ�ӦΪ���ڱ��ڢ�A��Ԫ�أ�Z�����Ϊ+6�ۣ�ӦΪSԪ�أ�Q�����ۣ�ӦΪOԪ�أ�Y�Ļ��ϼ�Ϊ+3�ۣ�ӦΪ���ڱ��ڢ�A��Ԫ�أ����ݰ뾶����ZС��X��֪Ӧ��Xͬ���ڣ�ΪAlԪ�أ�RΪ+1�ۣ���ԭ�Ӱ뾶С��O����RΪHԪ�أ�Ȼ����Ԫ��������֪ʶ�����⣮
���
�⣺X��M�Ļ��ϼ۶�Ϊ+2�ۣ�ӦΪ���ڱ��ڢ�A�壬���ݰ뾶��ϵ��֪MΪBe��XΪMg��Z��Q�Ļ��ϼ۶���-2�ۣ�ӦΪ���ڱ��ڢ�A��Ԫ�أ�Z�����Ϊ+6�ۣ�ӦΪSԪ�أ�Q�����ۣ�ӦΪOԪ�أ�Y�Ļ��ϼ�Ϊ+3�ۣ�ӦΪ���ڱ��ڢ�A��Ԫ�أ����ݰ뾶����ZС��X��֪Ӧ��Xͬ���ڣ�ΪAlԪ�أ�RΪ+1�ۣ���ԭ�Ӱ뾶С��O����Rֻ��λ�ڵ�һ���ڣ���RΪHԪ�أ�
��1��ZΪSԪ�أ�ԭ������Ϊ16��λ�����ڱ��е�3���ڢ�A�壬
�ʴ�Ϊ����3���ڢ�A�壻
��2��X��Y��Q�ֱ�ΪMg��Al��OԪ�أ���Ӧ���ӵĵ��Ӳ㶼��2����ԭ������ԽС�����Ӱ뾶Խ���������Ӱ뾶����ΪO2-��
�ʴ�Ϊ��O2-��
��3��MΪBe������Al�������Ƶ����ʣ���BeO���������Ʒ�Ӧ�����ӷ���ʽΪ��BeO+2OH-=BeO22-+H2O��
�ʴ�Ϊ��BeO+2OH-=BeO22-+H2O��
��4����Q��R��ԭ�Ӹ�����1��1��ɵĻ������ΪH2O2��˫��ˮ�����к��зǼ��Թ��ۼ��ͼ��Թ��ۼ���
�ʴ�Ϊ�����Թ��ۼ��ͷǼ��Թ��ۼ���
��b���ӵĵ�������õ���������˫��ˮ���缫��ӦΪ��O2+2e-+2H2O=H2O2+2OH-���÷�ӦΪ��ԭ��Ӧ����bΪ��Դ������aΪ������
�ʴ�Ϊ��������O2+2e-+2H2O=H2O2+2OH-��
��1��ZΪSԪ�أ�ԭ������Ϊ16��λ�����ڱ��е�3���ڢ�A�壬
�ʴ�Ϊ����3���ڢ�A�壻
��2��X��Y��Q�ֱ�ΪMg��Al��OԪ�أ���Ӧ���ӵĵ��Ӳ㶼��2����ԭ������ԽС�����Ӱ뾶Խ���������Ӱ뾶����ΪO2-��
�ʴ�Ϊ��O2-��
��3��MΪBe������Al�������Ƶ����ʣ���BeO���������Ʒ�Ӧ�����ӷ���ʽΪ��BeO+2OH-=BeO22-+H2O��
�ʴ�Ϊ��BeO+2OH-=BeO22-+H2O��
��4����Q��R��ԭ�Ӹ�����1��1��ɵĻ������ΪH2O2��˫��ˮ�����к��зǼ��Թ��ۼ��ͼ��Թ��ۼ���
�ʴ�Ϊ�����Թ��ۼ��ͷǼ��Թ��ۼ���
��b���ӵĵ�������õ���������˫��ˮ���缫��ӦΪ��O2+2e-+2H2O=H2O2+2OH-���÷�ӦΪ��ԭ��Ӧ����bΪ��Դ������aΪ������
�ʴ�Ϊ��������O2+2e-+2H2O=H2O2+2OH-��
���������⿼����λ�á��ṹ�����ʹ�ϵ���ۺ�Ӧ�ã���Ŀ�Ѷ��еȣ������漰Ԫ���ƶϡ����ӷ���ʽ����д�����ԭ����Ӧ�õ�֪ʶ������֪ʶ��϶ࡢ�ۺ��Խ�ǿ����ֿ�����ѧ����ѧ���ķ������������������Ӧ�û���֪ʶ��������

��ϰ��ϵ�д�
�����Ŀ
��SO2����ͨ��BaCl2 ��Һ�У�û�п�������������ͨ��һ�����壨�����һ�����ʣ�������һ�ְ�ɫ�����������壨�����ʣ��������ǣ�������
| A��Cl2 |
| B��CO2 |
| C��NH3 |
| D��SO3 |
����ͼʾ��ʵ�����������ʵ����Ӧʵ��Ŀ���ǣ�������
| A����ױ��뼺�� | B�о�Ũ�ȶ�Fe3++3SCN-?Fe��SCN��3 ��Ӱ�� |
 |  |
| C����CH3CH2OH��ŨH2SO4������170��IJ�����ϩ | D�Ƚ�̼������̼�����Ƶ����ȶ��� |
 |  |
| A��A | B��B | C��C | D��D |
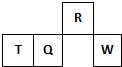 ������Ԫ��R��T��Q��W��Ԫ�����ڱ��е����λ����ͼ��ʾ������T�ǵؿ��к������Ľ���Ԫ�أ������жϵ���ȷ�ǣ�������
������Ԫ��R��T��Q��W��Ԫ�����ڱ��е����λ����ͼ��ʾ������T�ǵؿ��к������Ľ���Ԫ�أ������жϵ���ȷ�ǣ�������| A�������̬�⻯������ȶ��ԣ�Q��R |
| B������������Ӧˮ��������ԣ�Q��W |
| C��ԭ�Ӱ뾶��T��Q��R |
| D����TԪ�ص�����Һһ�������� |
�����Լ��У�����������FeCl3������Լ��ǣ�������
| A��NaNO3��Һ |
| B��ϡ���� |
| C��KSCN��Һ |
| D������KMnO4��Һ |
 ��ʾ���������й�˵����ȷ���ǣ�˫ѡ��
��ʾ���������й�˵����ȷ���ǣ�˫ѡ��
 ����һ�������£��������Ҳ����CO2���������ڻ�����C��CO2��Ӧ����D�ķ�Ӧ���������ֻ������Ϊͬ���칹�壩��д����������һ�ֻ�����Ľṹ��ʽ��
����һ�������£��������Ҳ����CO2���������ڻ�����C��CO2��Ӧ����D�ķ�Ӧ���������ֻ������Ϊͬ���칹�壩��д����������һ�ֻ�����Ľṹ��ʽ�� ��Ѫ��������ʳ���е������ڵ���ʽ֮һ����Ҫ���������뵰���ʺ������ϳ�����
��Ѫ��������ʳ���е������ڵ���ʽ֮һ����Ҫ���������뵰���ʺ������ϳ�����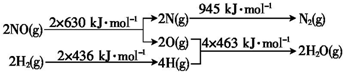 H2��ԭNO���ɵ�����ˮ�������Ȼ�ѧ����ʽ��
H2��ԭNO���ɵ�����ˮ�������Ȼ�ѧ����ʽ��