题目内容
13.下列化学事实及其解释都正确的是( )| A. | 滴有酚酞的碳酸氢钠溶液显红色,微热后红色加深,是因为碳酸氢钠分解生成了碳酸钠 | |
| B. | 用洁净的玻璃管向包有过氧化钠的脱脂棉吹气,脱脂棉燃烧,说明二氧化碳、水与过氧化钠的反应是放热反应 | |
| C. | 向溴水中滴入植物油,振荡后油层显无色,说明溴不溶于油脂 | |
| D. | 粗锌与稀硫酸反应制氢气比纯锌快,是因为粗锌比纯锌还原性强 |
分析 A.碳酸氢钠溶液中存在水解平衡,微热促进水解,氢氧根离子浓度增大;
B.CO2、H2O与Na2O2反应,为放热反应,且生成氧气;
C.植物油中含C=C,与溴水发生加成反应;
D.粗锌与硫酸构成原电池,加快反应速率.
解答 解:A.碳酸氢钠溶液中存在水解平衡,微热促进水解,氢氧根离子浓度增大,与水解平衡有关,不涉及碳酸氢钠的分解,故A错误;
B.CO2、H2O与Na2O2反应,为放热反应,且生成氧气,则用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧,故B正确;
C.植物油中含C=C,与溴水发生加成反应,则向溴水中滴入植物油,振荡后,褪色,不能说明溶解性,故C错误;
D.粗锌与硫酸构成原电池,加快反应速率,与还原性无关,故D错误;
故选B.
点评 本题考查化学实验方案的评价,涉及盐类水解等、原电池与化学反应速率、物质的性质等,侧重化学反应原理和物质性质的考查,选项D为易错点,题目难度中等.

练习册系列答案
相关题目
3.下列叙述正确的是( )
| A. | 1molH2O的质量为18g/mol | B. | CH4的摩尔质量为16g | ||
| C. | 3.01×1023个SO2分子的质量为32g | D. | 0.05mol SO2的体积是1.12L |
4.奥运会篮球比赛用球男女有别.男子篮球比赛用7#球,内部空间体积大约是7.35L,比赛时内部压强约为170kPa.
己知,在25℃,100kPa时,气体摩尔体积约为24.5L/mol.假设比赛场馆温度为25℃,下列说法中正确的是( )
己知,在25℃,100kPa时,气体摩尔体积约为24.5L/mol.假设比赛场馆温度为25℃,下列说法中正确的是( )
| A. | 比赛时,篮球内一般充填氮气 | B. | 比赛时,篮球内约有空气0.3mol | ||
| C. | 比赛时,篮球内约有空气14.8g | D. | 当25℃,170kPa时,Vm>24.5L/mol |
1.下列说法正确的是( )
| A. | 124g P4含有的P-P键数为4NA(设NA表示阿伏伽德罗常数的值) | |
| B. | Be和NaOH溶液反应的离子方程式是:2Be+2OH -+2H2O=2BeO2-+3H2↑ | |
| C. | 在NaCl溶液中加入AgNO3溶液,生成白色沉淀;再加入氨水,沉淀消失,沉淀消失发生的离子方程式是: AgCl+2NH3•H2O=[Ag(NH3)2]++Cl-+2H2O | |
| D. | 0.1mol/L的Fe3+溶液中,能大量共存的离子有Cl-、SO42-、SCN- |
8.将0.5mol NaCl固体溶解于水,制得NaCl的物质的量浓度为2mol/L溶液,则溶液的体积为( )
| A. | 100 mL | B. | 250 mL | C. | 400 mL | D. | 1000 mL |
18.下列有关说法错误的是( )
| A. | 为保护海轮的船壳,常在船壳上镶入锌块 | |
| B. | 纯碱溶于热水中,去污效果增强,说明纯碱的水解反应是吸热反应 | |
| C. | 已知工业合成氨△H<O,达平衡后,升高温度,正反应速率减少、逆反应速率增大,平衡向逆反应方向移动 | |
| D. | NH3(g)+HCl(g)═NH4Cl(s)较低温下能自发进行,说明该反应的△H<O |
5.在甲烧杯中放入盐酸,乙烧杯中放入醋酸,两种溶液的体积和pH都相等,向两烧杯中同时加入质量不等的锌粒,反应结束后得到等量的氢气.下列说法正确的是( )
| A. | 甲烧杯中放入锌的质量比乙烧杯中放入锌的质量大 | |
| B. | 甲烧杯中的酸过量 | |
| C. | 甲烧杯比乙烧杯反应快 | |
| D. | 反应开始后乙烧杯中的c(H+)始终比甲烧杯中的c(H+)小 |
2.下列化学用语正确的是( )
| A. | 硫离子的结构示意图: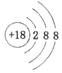 | B. | FeSO3的名称是亚硫酸铁 | ||
| C. | 电子转移情况: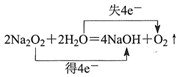 | D. | 氮气分子的电子式: |
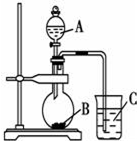 某研究性学习小组设计了一组实验验证元素周期律.
某研究性学习小组设计了一组实验验证元素周期律.