题目内容
 某研究性学习小组设计实验方案(见图)研究稀硝酸与铜反应生成NO.
某研究性学习小组设计实验方案(见图)研究稀硝酸与铜反应生成NO.(1)补充完成下列实验步骤:
①按图连接好装置
②
③打开活塞A,往U型管右侧漏斗中注入稀硝酸,一直注到稀HNO3接触到A处橡皮塞为止;
④关闭活塞A,观察实验现象.
(2)记录:
可观察到的现象有:
(3)要验证生成的气体是NO,其具体操作及现象是
(4)试管内装有NO,倒置于水槽中,当向试管内通入21mL O2时,最后试管中的液面仍在原的位置,则原试管中NO的体积为
考点:实验装置综合
专题:实验题
分析:(1)因反应生成气体,则连接好仪器之后需要检查气密性;
(2)铜和稀硝酸反应生成硝酸铜和一氧化氮气体,溶液呈蓝色;
(3)根据一氧化氮和氧气反应生成红综合二氧化氮判断;
(4)最后试管中的液面仍在原的位置,说明反应后氧气的体积等于原试管中NO的体积,结合反应4NO+O2+2H2O=4HNO3计算.
(2)铜和稀硝酸反应生成硝酸铜和一氧化氮气体,溶液呈蓝色;
(3)根据一氧化氮和氧气反应生成红综合二氧化氮判断;
(4)最后试管中的液面仍在原的位置,说明反应后氧气的体积等于原试管中NO的体积,结合反应4NO+O2+2H2O=4HNO3计算.
解答:
解:(1)因反应生成气体,则连接好仪器之后需要检查气密性,故答案为:检查装置气密性;
(2)铜和稀硝酸反应生成硝酸铜和一氧化氮气体,反应的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,溶液呈蓝色,可观察到的现象是铜丝逐渐溶解,产生无色气体,U形管左侧液面下降,溶液显蓝色,
故答案为:铜丝逐渐溶解,产生无色气体,U形管左侧液面下降,溶液显蓝色;3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
(3)一氧化氮为无色气体,如检验是否生成一氧化氮,则可打开活塞A,一氧化氮和空气接触生成二氧化氮,在球形干燥管里看到气体显红色,则说明原气体为NO,
故答案为:打开活塞A,在球形干燥管里看到气体显红色,则说明原气体为NO;
(4)最后试管中的液面仍在原的位置,说明反应后氧气的体积等于原试管中NO的体积,
设原试管中NO的体积为VmL,
则4NO+3O2+2H2O=4HNO3,
4 3
VmL
mL,
则21mL-
mL=VmL,
V=12,
故答案为:12.
(2)铜和稀硝酸反应生成硝酸铜和一氧化氮气体,反应的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,溶液呈蓝色,可观察到的现象是铜丝逐渐溶解,产生无色气体,U形管左侧液面下降,溶液显蓝色,
故答案为:铜丝逐渐溶解,产生无色气体,U形管左侧液面下降,溶液显蓝色;3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
(3)一氧化氮为无色气体,如检验是否生成一氧化氮,则可打开活塞A,一氧化氮和空气接触生成二氧化氮,在球形干燥管里看到气体显红色,则说明原气体为NO,
故答案为:打开活塞A,在球形干燥管里看到气体显红色,则说明原气体为NO;
(4)最后试管中的液面仍在原的位置,说明反应后氧气的体积等于原试管中NO的体积,
设原试管中NO的体积为VmL,
则4NO+3O2+2H2O=4HNO3,
4 3
VmL
| 3V |
| 4 |
则21mL-
| 3V |
| 4 |
V=12,
故答案为:12.
点评:本题以硝酸与铜的反应为载体,综合考查学生实验设计和探究能力,涉及HNO3的性质、物质验证性实验设计,利用对比的方法判断硝酸的性质,题目难度中等,是对基础知识与学生综合能力的考查,理解原理与各装置作用是解题的关键.

练习册系列答案
相关题目
下列事实不能用勒夏特列原理解释的是( )
| A、红棕色NO2加压后颜色先变深后变浅 |
| B、实验室中常用排饱和食盐水的方法收集氯气 |
| C、SO2催化氧化成SO3的反应,使用过量的空气以提高二氧化硫的利用率 |
| D、压缩H2与I2(g)反应的平衡混合气体,颜色变深 |
下列各组元素按电负性大小排列正确的是( )
| A、F>N>O |
| B、O>Cl>F |
| C、As>P>H |
| D、Cl>S>As |
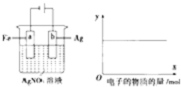 按如图装置实验,若x轴表示流入阴极的电子的物质的量,则y轴可表示( )
按如图装置实验,若x轴表示流入阴极的电子的物质的量,则y轴可表示( )①c(Ag+) ②c(AgNO3) ③a棒的质量 ④b棒的质量 ⑤溶液的质量.
| A、①③ | B、③④ |
| C、①②④ | D、①②⑤ |
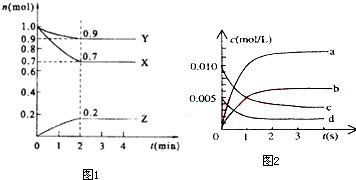
 Ⅰ.在t℃时,某NaOH稀溶液中,c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,则:
Ⅰ.在t℃时,某NaOH稀溶液中,c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,则: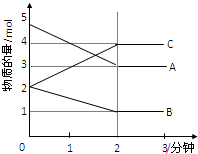 某可逆反应在某体积为5L的密闭容器中进行,在从0-3分钟各物质的量的变化情况如图所示(A,B,C均为气体).
某可逆反应在某体积为5L的密闭容器中进行,在从0-3分钟各物质的量的变化情况如图所示(A,B,C均为气体).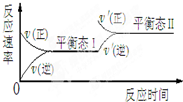 随着人类对温室效应和资源短缺等问题的重视,降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.目前有一种方法是用CO2来生产燃料甲醇CH3OH.在体积不变的5L密闭容器中,充入一定量的CO2和 H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g);(正反应为放热反应)经过10min反应达到平衡,测得物质的浓度如下表所示.
随着人类对温室效应和资源短缺等问题的重视,降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.目前有一种方法是用CO2来生产燃料甲醇CH3OH.在体积不变的5L密闭容器中,充入一定量的CO2和 H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g);(正反应为放热反应)经过10min反应达到平衡,测得物质的浓度如下表所示.