题目内容
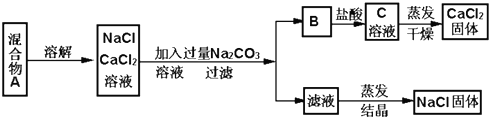
(1)一学生设计了如下实验方法分离NaCl和CaCl2两种固体混合物
填空和回答下列问题
①B物质是 (写化学式)
②按此实验方案分离得到的NaCl,经分析含有杂质,是因为上述方案中某一步设计有错误,这一步的正确设计方案应是 .
③蒸发结晶用到的主要仪器有 .
④若要测定该样品中NaCl和CaCl2的质量比,可称量干燥的B物质和另一物质的质量,这种物质是 .
(2)实验室配制250mL 1mol?L-1的氢氧化钠溶液的实验步骤如下:
a.计算需要氢氧化钠固体的质量.
b.称量氢氧化钠固体.
c.将烧杯中的溶液注入某容器中,并用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也注入该容器中.
d.用适量的蒸馏水溶解称量好的氢氧化钠固体,冷却至室温.
e.盖好瓶塞,反复上下颠倒,摇匀.
f.继续向某容器中加蒸馏水至刻度线下1~2cm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切.
回答下列问题:
①需称量 g的氢氧化钠.
②上述步骤的正确操作顺序是 (填序号).
③上述实验,除用到托盘天平、烧杯、胶头滴管、药匙、玻璃棒外,还需要一种重要的仪器是 .
④若定容时俯视刻度,则会使所配氢氧化钠溶液的浓度 .(填“偏大”或“偏小”)

填空和回答下列问题
①B物质是
②按此实验方案分离得到的NaCl,经分析含有杂质,是因为上述方案中某一步设计有错误,这一步的正确设计方案应是
③蒸发结晶用到的主要仪器有
④若要测定该样品中NaCl和CaCl2的质量比,可称量干燥的B物质和另一物质的质量,这种物质是
(2)实验室配制250mL 1mol?L-1的氢氧化钠溶液的实验步骤如下:
a.计算需要氢氧化钠固体的质量.
b.称量氢氧化钠固体.
c.将烧杯中的溶液注入某容器中,并用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也注入该容器中.
d.用适量的蒸馏水溶解称量好的氢氧化钠固体,冷却至室温.
e.盖好瓶塞,反复上下颠倒,摇匀.
f.继续向某容器中加蒸馏水至刻度线下1~2cm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切.
回答下列问题:
①需称量
②上述步骤的正确操作顺序是
③上述实验,除用到托盘天平、烧杯、胶头滴管、药匙、玻璃棒外,还需要一种重要的仪器是
④若定容时俯视刻度,则会使所配氢氧化钠溶液的浓度
考点:物质分离、提纯的实验方案设计,配制一定物质的量浓度的溶液
专题:
分析:(1)分离NaCl和CaCl2两种固体混合物,溶解后加入过量碳酸钠溶液,生成碳酸钙沉淀和氯化钠,碳酸钙和盐酸发生CaCO3+2H+=Ca2++CO2↑+H2O,得到氯化钙溶液,经蒸发可得到氯化钙固体;由于碳酸钠过量,所以滤液中的物质有氯化钠和碳酸钠,因此要得到纯净的氯化钠就需要除去碳酸钠,加入稀盐酸最合适,碳酸钠和稀盐酸生成氯化钠和水和二氧化碳,蒸发后最后的固体物质是氯化钠;
(2)①结合m=cVM计算;
②根据实验操作的步骤(计算→称量→溶解、冷却→移液→洗涤→定容→摇匀),进行操作顺序的排序;
③根据实验操作的步骤以及每步操作需要仪器确定反应所需仪器分析;
④定容时俯视刻度,溶液体积V偏小,结合c=
分析.
(2)①结合m=cVM计算;
②根据实验操作的步骤(计算→称量→溶解、冷却→移液→洗涤→定容→摇匀),进行操作顺序的排序;
③根据实验操作的步骤以及每步操作需要仪器确定反应所需仪器分析;
④定容时俯视刻度,溶液体积V偏小,结合c=
| n |
| V |
解答:
解:(1)①NaCl和CaCl2两种固体混合物,溶解后加入过量碳酸钠溶液,生成碳酸钙沉淀和氯化钠,过滤后得到的沉淀B为碳酸钙,故答案为:CaCO3;
②由于碳酸钠过量,所以滤液中的物质有氯化钠和碳酸钠,因此要得到纯净的氯化钠就需要除去碳酸钠,向滤液中加入适量盐酸至不产生气体,生成氯化钠和水和二氧化碳,蒸发后最后的固体物质是氯化钠,
故答案为:先加入适量盐酸至不产生气体后再蒸发结晶;
③蒸发需要的主要仪器为:铁架台,酒精灯,蒸发皿,玻璃棒;
故答案为:铁架台、酒精灯、蒸发皿、玻璃棒;
④要测定该样品中NaCl和CaCl2的质量比,可称量干燥的碳酸钙的质量,根据反应CaCO3+2H+=Ca2++CO2↑+H2O可计算氯化钙的质量,混合物A的总质量减去氯化钙的质量可得氯化钠的质量,
故答案为:混合物A;
(2)①NaOH的质量为0.25L×1mol/L×40g/mol=10.0g,故答案为:10.0;
②配制一定物质的量浓度的溶液的配制顺序是:计算→称量→溶解、冷却→移液→洗涤→定容→摇匀,故正确的操作顺序为abdcfe,故答案为:abdcfe;
③配制一定物质的量浓度的溶液需要的仪器为:托盘天平、烧杯、胶头滴管、药匙、玻璃棒、250mL容量瓶,故答案为:250mL容量瓶;
④定容时俯视刻度,溶液体积V偏小,由c=
可知,所配氢氧化钠溶液的浓度偏大,故答案为:偏大.
②由于碳酸钠过量,所以滤液中的物质有氯化钠和碳酸钠,因此要得到纯净的氯化钠就需要除去碳酸钠,向滤液中加入适量盐酸至不产生气体,生成氯化钠和水和二氧化碳,蒸发后最后的固体物质是氯化钠,
故答案为:先加入适量盐酸至不产生气体后再蒸发结晶;
③蒸发需要的主要仪器为:铁架台,酒精灯,蒸发皿,玻璃棒;
故答案为:铁架台、酒精灯、蒸发皿、玻璃棒;
④要测定该样品中NaCl和CaCl2的质量比,可称量干燥的碳酸钙的质量,根据反应CaCO3+2H+=Ca2++CO2↑+H2O可计算氯化钙的质量,混合物A的总质量减去氯化钙的质量可得氯化钠的质量,
故答案为:混合物A;
(2)①NaOH的质量为0.25L×1mol/L×40g/mol=10.0g,故答案为:10.0;
②配制一定物质的量浓度的溶液的配制顺序是:计算→称量→溶解、冷却→移液→洗涤→定容→摇匀,故正确的操作顺序为abdcfe,故答案为:abdcfe;
③配制一定物质的量浓度的溶液需要的仪器为:托盘天平、烧杯、胶头滴管、药匙、玻璃棒、250mL容量瓶,故答案为:250mL容量瓶;
④定容时俯视刻度,溶液体积V偏小,由c=
| n |
| V |
点评:本题考查物质的分离、提纯知识及溶液配制,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握实验的原理和操作方法为解答该题的关键,题目难度不大.

练习册系列答案
相关题目
下列离子方程式正确的是( )
| A、向盐酸中滴加氨水:H++NH3?H2O=H2O+NH4+ |
| B、Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
| C、铜溶于稀硝酸:3Cu+8H++2NO3-=3Cu2++2 NO↑+4H2O |
| D、向Na2S2O3溶液中通入足量氯气:S2O32-+2Cl2+3H2O=2SO32-+4Cl-+6H+ |
已知:Cu2O+2H+═Cu2++Cu+H2O;3Cu+8HNO3(稀)
3Cu(NO3)2+2NO↑+4H2O,为检验某金属铜粉末样品中是否含有Cu2O,某同学设计了如下方案,其中不合理的是( )
| ||
| A、将足量CO通过灼热样品,冷却后称量,若固体质量减小,则含有Cu2O |
| B、将干燥的H2通过灼热样品,再通过无水硫酸铜,若无水硫酸铜变蓝,则含有Cu2O |
| C、取少量样品,加入稀硝酸,充分振荡后若观察到溶液呈蓝色,则含有Cu2O |
| D、取少量样品,加入稀硫酸,充分振荡后若观察到溶液呈蓝色,则含有Cu2O |
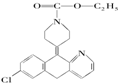 开瑞坦是治疗过敏性鼻炎的良药,其有效成分的结构简式如图所示,下列关于该有机物的说法正确的是( )
开瑞坦是治疗过敏性鼻炎的良药,其有效成分的结构简式如图所示,下列关于该有机物的说法正确的是( )| A、该有机物的分子式是C21H22N2O2Cl |
| B、分子中含有四个六元环,其中有一个是苯环 |
| C、1mol分子发生水解反应后能得到2mol新分子 |
| D、1mol分子发生加成反应需要8molH2 |

