题目内容
10.电解法降解NO3-的原理如图所示,电解总反应为4NO3-+4H+$\frac{\underline{\;通电\;}}{\;}$2N2↑++5O2↑+2H2O.下列说法正确的是( )
| A. | 电子通过盐桥向正极方向移动 | |
| B. | 电源的正极反应式为AsO43-+2H++2e-═AsO33-+H2O | |
| C. | 导线中流过1 mol e-时,理论上有1.2 mol H+通过质子交换膜 | |
| D. | Ag-Pt电极附近溶液的pH减小 |
分析 左边是原电池,右边是电解池,电解池的左边是NO3-得到电子被还原为N2,电极反应式为2NO3-+6H2O+10e-=N2↑+12OH-;
则质子交换膜的左边是阴极,与阴极相连的惰性电极是原电池的负极,是I-失电子被氧化成I2,原电池的正极AsO43-得电子被还原为AsO33-,
A.有盐桥的是原电池,盐桥中是阴离子向负极称动,阳离子向正极移动;
B.原电池为电源,反应中元素化合价变化分析,生成氮气的电极为电解池电解池阴极,连接原电池负极,原电池左侧电极为正极,AsO43-在酸性溶液中被还原为AsO33-;
C.依据电极反应电子守恒计算得到通过质子交换膜的氢离子物质的量;
D.Ag-Pt电极为电解质的阴极,电极反应式为2NO3-+6H2O+10e-=N2↑+12OH-.
解答 解:A.左边是原电池,右边是电解池,盐桥中是阴离子向负极称动,阳离子向正极移动,电子不能通过盐桥,故A错误;
B.原电池为电源,反应中元素化合价变化分析,生成氮气的电极为电解池电解池阴极,连接原电池负极,原电池左侧电极为正极,AsO43-在酸性溶液中被还原为AsO33-,电极反应为:AsO43-+2H++2e-═AsO33-+H2O,故B正确;
C.依据原电池正极电极反应AsO43-+2H++2e-═AsO33-+H2O,导线中流过1 mol e-时,理论上有1 mol H+通过质子交换膜,故C错误;
D.Ag-Pt电极为电解质的阴极,电极反应式为2NO3-+6H2O+10e-=N2↑+12OH-,电极附近溶液PH增大,故D错误;
故选B.
点评 本题考查了原电池、电解池原理的分析应用,主要是电极名称、电极反应方程式等知识点,掌握基础是解题关键,题目难度中等.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
10.下列各项表述中正确的是( )
| A. | I-131的原子组成:5378I | B. | HCl电子式: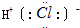 | ||
| C. | Na2S的电子式: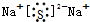 | D. | D2O的摩尔质量为:18g/mol |
11.有乙烯与乙炔的混合气体100mL,与280mL氧气充分反应,完全燃烧后生成二氧化碳的体积(以上气体体积均在相同状况下测定)
| A. | 小于200mL | B. | 200mL | C. | 大于200mL | D. | 无法确定 |
8.从海水中提取溴有如下反应:5NaBr+NaBrO3+3H2SO4═3Br2+Na2SO4+3H2O,与上述反应在氧化还原反应原理上最相似的是( )
| A. | 3Cl2+6NaOH=2NaClO3+5NaCl+3H2O | |
| B. | CaH2+2H2O=Ca(OH)2+2H2↑ | |
| C. | AlCl3+3NaAlO2+6H2O=4Al(OH)3↓+3NaCl | |
| D. | 2CuO+Cu2S=4Cu+SO2↑ |
5.下列说法正确的是( )
| A. | 由不同原子组成的纯净物一定是化合物 | |
| B. | 一定温度和压强下,30 L某种气态纯净物中含有6.02×1023个分子,这些分子由1.204×1024个原子组成,则该气体中每个分子含有2个原子 | |
| C. | 含金属元素的离子一定都是阳离子 | |
| D. | 胆矾是混净物,水泥是混合物 |
15.现有部分短周期元素的性质或原子结构如表且原子序数按XYTZ依次增大:
(1)四种元素原子半径由大到小的顺序是(写元素符号)S>Cl>C>N.
(2)元素Y与氢元素形成的一种离子YH4+,写出该微粒的电子式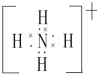 (用元素符号表示).
(用元素符号表示).
(3)T元素的简单阴离子的结构示意图是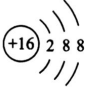 ,
,
(4)证明该粒子的还原性比Z-强的离子方程式是Cl2+S2-=S+2Cl-.
(5)元素Z的单质与氢氧化钠溶液反应的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O.
(6)将9g单质X在足量氧气中燃烧,所得气体通入1L 1mol•L-1NaOH溶液中,完全吸收后,将溶液在减压低温条件下蒸干,得到不含结晶水的固体质量为68.5g.
| 元素编号 | 元素性质或原子结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| T | 最外层电子数是电子层数的2倍 |
| Z | 元素最高正价是+7价 |
(2)元素Y与氢元素形成的一种离子YH4+,写出该微粒的电子式
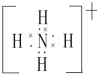 (用元素符号表示).
(用元素符号表示).(3)T元素的简单阴离子的结构示意图是
 ,
,(4)证明该粒子的还原性比Z-强的离子方程式是Cl2+S2-=S+2Cl-.
(5)元素Z的单质与氢氧化钠溶液反应的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O.
(6)将9g单质X在足量氧气中燃烧,所得气体通入1L 1mol•L-1NaOH溶液中,完全吸收后,将溶液在减压低温条件下蒸干,得到不含结晶水的固体质量为68.5g.
2.在H2O、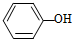
 、CH 3COOH、HCl的排列中,
、CH 3COOH、HCl的排列中, 应填入的物质是( )
应填入的物质是( )

 、CH 3COOH、HCl的排列中,
、CH 3COOH、HCl的排列中, 应填入的物质是( )
应填入的物质是( )| A. | H2SO4 | B. | CH3CH2OH | C. | H2CO3 | D. | CH3COOCH3 |
19.将淀粉加入试管里,加适量的水,振荡,加热煮沸,取所得溶液3mL,加1mL 稀硫酸溶液,加热一分钟,冷却后加入新制的Cu(OH)2悬浊液,加热后未见红色沉淀,其原因是( )
| A. | 加入Cu(OH)2浊液之前,未用NaOH溶液中和硫酸 | |
| B. | 制Cu(OH)2时,硫酸铜溶液太稀,NaOH过量了 | |
| C. | 加热时间不充分,淀粉没有充分水解 | |
| D. | 所用淀粉浓度不够 |
20.下列各组离子,在强碱性溶液中可以大量共存的是( )
| A. | K+、Na+、HSO3-、Cl- | B. | H+、Al3+、Fe3+、I- | ||
| C. | NH4+、K+、Cl-、NO3- | D. | Na+、Ba2+、AlO2-、NO3- |