题目内容
9.等体积、等物质的量浓度的氢硫酸H2S和硫酸溶液中,存在的离子总数的关系是( )| A. | H2S中多 | B. | H2SO4中多 | C. | 一样多 | D. | 无法比较 |
分析 氢硫酸H2S和硫酸是二元酸,氢硫酸为二元弱酸,溶液中分步电离,硫酸为二元强酸,溶液中完全电离,据此分析计算所含的离子总数;
解答 解:等体积、等物质的量浓度的氢硫酸H2S和硫酸溶液中,溶质物质的量相同,氢硫酸H2S和硫酸是二元酸,氢硫酸为二元弱酸,溶液中分步电离,H2S?H++HS-,HS-?H++S2-,溶液中存在的离子为:H+、HS-、S2-、OH-,但电离程度较小,主要是以H2S分子形式存在,硫酸为二元强酸,溶液中完全电离,H2SO4=2H++SO42-,所以溶液中离子总数硫酸中多,
故选B.
点评 本题考查了强弱电解质的电离过程分析,注意弱电解质溶液中存在电离平衡且电离程度很小,强电解质完全电离,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列有关试剂的保存方法,错误的是( )
| A. | 浓硝酸保存在棕色玻璃试剂瓶中 | |
| B. | 少量的钠保存在煤油中 | |
| C. | 新制的氯水通常保存在棕色玻璃试剂瓶中 | |
| D. | 氢氧化钠溶液用带磨口玻璃塞的普通试剂瓶贮存 |
17.制备下列有机化合物时,常会混有括号内的杂质,以下除杂方法正确的是( )
| A. | 苯(甲苯):加酸性高锰酸钾溶液、再加NaOH溶液,分液 | |
| B. | 乙烷(乙烯),催化条件下通入H2 | |
| C. | 乙酸(乙醛),加入新制氢氧化铜,蒸馏 | |
| D. | 乙醛(乙酸),加入氢氧化钠溶液洗涤,蒸馏 |
1.下列实验操作中,正确的是( )
| A. | 在蒸发皿中放入NaCl溶液,加热NaCl溶液制取NaCl晶体 | |
| B. | 用100mL的量筒量取5.2mL的盐酸 | |
| C. | 用托盘天平称取25.20gNaCl | |
| D. | 用酒精萃取溴水中的溴单质 |
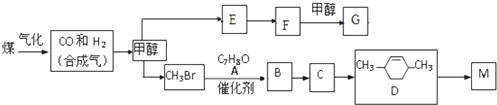
 +RX$\stackrel{催化剂}{→}$
+RX$\stackrel{催化剂}{→}$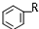 +HX完成下列填空:
+HX完成下列填空: 2HCHO+2H2O.
2HCHO+2H2O.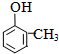 .
.