题目内容
6.一定条件下反应:2SO2+O2?2SO3 发生时,能使V(SO2)增大的措施有( )①增大压强 ②降低压强 ③通入SO2 ④增加的O2量 ⑤升高温度 ⑥降低温度.
| A. | ①②③⑤ | B. | ②③④⑥ | C. | ②③④⑤ | D. | ①③④⑤ |
分析 一般来说,升高温度、加入催化剂、增大浓度可增大反应速率,反之降低反应速率,以此解答该题.
解答 解:①增大压强,浓度增大,反应速率增大,故正确;
②降低压强,浓度减小,反应速率减小,故错误;
③通入SO2,反应物浓度增大,反应速率增大,故正确;
④增加的O2量,反应物浓度增大,反应速率增大,故正确;
⑤升高温度,反应速率增大,故正确;
⑥降低温度,反应速率减小,故错误.
故选D.
点评 本题考查化学反应速率的影响因素,为高频考点,侧重于学生的分析能力的考查,难度不大,注意相关基础知识的积累即可解答该题.

练习册系列答案
相关题目
14.下列离子方式书写正确的是( )
| A. | 已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量CO2 2ClO-+CO2+H2O=2HClO+CO32- | |
| B. | 向沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O=Fe(OH)3↓+3H+ | |
| C. | Na2S溶液中滴加NaClO溶液:S2-+ClO-+H2O=S↓+Cl-+2OH- | |
| D. | 将少量SO2气体通入NaClO溶液中:SO2+H2O+2ClO-═SO32-+2HClO |
1.下列解释事实的离子方程式正确的是( )
| A. | 铁和稀硝酸反应制得浅绿色溶液:Fe+4H++NO3-═Fe3++NO↑+2H2O | |
| B. | 在NaClO溶液中通入过量SO2气体:ClO-+H2O+SO2═HClO+HSO3- | |
| C. | NaHCO3与少量Ca(OH)2溶液反应:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- | |
| D. | 10mL 0.5mol/L的明矾溶液与20mL 0.5mol/L的Ba(OH)2溶液混合反应:3Ba2++6OH-+2Al3++3SO42-═3BaSO4↓+2Al(OH)3↓ |
18.为提纯下列物质(括号内为杂质)选用的试剂和分离方法都正确的是( )
| 序号 | 物质 | 试剂 | 分离方法 |
| ① | 硝酸钾(氯化钠) | 蒸馏水 | 重结晶 |
| ② | 二氧化碳(氯化氢) | 饱和碳酸钠溶液 | 洗气 |
| ③ | 乙醇(水) | 金属钠 | 蒸馏 |
| ④ | NaCl溶液(Na2S) | AgCl | 过滤 |
| A. | ①③ | B. | ①④ | C. | ② | D. | ③④ |
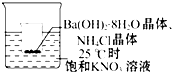 把小烧杯放入25℃的盛有饱和硝酸钾溶液的大烧杯中,小烧杯(已被设法固定)中放有 25g研成粉末的氢氧化钡晶体[Ba(OH)2•8H2O],再加入约12g的氯化铵晶体,并搅拌使其充分反应.
把小烧杯放入25℃的盛有饱和硝酸钾溶液的大烧杯中,小烧杯(已被设法固定)中放有 25g研成粉末的氢氧化钡晶体[Ba(OH)2•8H2O],再加入约12g的氯化铵晶体,并搅拌使其充分反应.