题目内容
铜片、锌片和200mL稀H2SO4组成的原电池中:
(1)正极电极反应式为 ;
(2)负极电极反应式为 ;
(3)若铜片上放出2.24L(标准状况下)的H2,H2SO4恰好用完,则产生这些气体消耗的Zn的质量为 克;
(4)原稀H2SO4溶液的物质的量浓度为 .
(1)正极电极反应式为
(2)负极电极反应式为
(3)若铜片上放出2.24L(标准状况下)的H2,H2SO4恰好用完,则产生这些气体消耗的Zn的质量为
(4)原稀H2SO4溶液的物质的量浓度为
考点:原电池和电解池的工作原理
专题:
分析:(1)原电池中不活泼金属做正极,发生得电子的还原反应;
(2)原电池中较活泼金属做负极,发生失电子的氧化反应;
(3)根据电极反应:2H++2e-═H2↑,当产生2.24L(标准状况)即0.1mol的气体时,转移电子为0.2mol进行计算;
(4)根据稀H2SO4溶液的物质的量浓度=
进行计算.
(2)原电池中较活泼金属做负极,发生失电子的氧化反应;
(3)根据电极反应:2H++2e-═H2↑,当产生2.24L(标准状况)即0.1mol的气体时,转移电子为0.2mol进行计算;
(4)根据稀H2SO4溶液的物质的量浓度=
| n |
| V |
解答:
解:(1)Zn、Cu、硫酸构成的原电池中,铜是正极,发生得电子的还原反应,电极反应:2H++2e-═H2↑,故答案为:2H++2e-═H2↑;
(2)Zn、Cu、硫酸构成的原电池中,金属锌做负极,发生失电子的氧化反应,反应式为:Zn-2e-=Zn2+,故答案为:Zn-2e-=Zn2+;
(3)根据电极反应:2H++2e-═H2↑,当产生2.24L(标准状况)即0.1mol的气体时,转移电子为0.2mol,则负极消耗0.1mol的锌,即0.1mol×65g/mol=6.5g,
故答案为:6.5;
(4)稀H2SO4溶液的物质的量浓度=
=
=0.5mol/L,故答案为:0.5mol/L.
(2)Zn、Cu、硫酸构成的原电池中,金属锌做负极,发生失电子的氧化反应,反应式为:Zn-2e-=Zn2+,故答案为:Zn-2e-=Zn2+;
(3)根据电极反应:2H++2e-═H2↑,当产生2.24L(标准状况)即0.1mol的气体时,转移电子为0.2mol,则负极消耗0.1mol的锌,即0.1mol×65g/mol=6.5g,
故答案为:6.5;
(4)稀H2SO4溶液的物质的量浓度=
| n |
| V |
| 0.1mol |
| 0.2L |
点评:本题考查学生原电池的工作原理及其计算,可注意归纳原电池工作原理规律,难度不大.

练习册系列答案
相关题目
下列物质中,在相同条件下最易与氢气化合的是( )
| A、F2 |
| B、Cl2 |
| C、Br2 |
| D、甲烷 |
NO和CO都是汽车尾气中的有害物质,它们能缓慢地反应生成氮气和二氧化碳,对此反应,下列叙述正确的是( )
| A、改变压强,不能改变该反应速率 |
| B、使用适当的催化剂能改变该反应速率 |
| C、升高温度不一定能提高该反应速率 |
| D、使用催化剂后,该反应速率之比不等于计量数之比了 |
为研究金属腐蚀的条件和速率,某课外小组学生用金属丝将三根大小相同的铁钉分别固定在如图所示的三个装置中,再放置于玻璃罩里保存相同的一段时间.下列实验结束时现象的描述不正确的是( )


| A、装置I左侧的铁钉一定会生锈 |
| B、左侧液面装置I比装置II的高 |
| C、装置II中的铁钉腐蚀最严重 |
| D、装置III中的铁钉几乎没有被腐蚀 |
 燃料电池是目前电池研究的热点之一.现有某课外小组自制的氢氧燃料电池,如图所示,a、b均为惰性电极.下列叙述不正确的是( )
燃料电池是目前电池研究的热点之一.现有某课外小组自制的氢氧燃料电池,如图所示,a、b均为惰性电极.下列叙述不正确的是( )| A、a极是负极,该电极上发生氧化反应 |
| B、b极反应是O2+4OH--4e-═2H2O |
| C、总反应方程式为2H2+O2═2H2O |
| D、氢氧燃料电池是一种具有应用前景的绿色电源 |
在2CuS+4H2SO4(浓)═2CuSO4+2SO2↑+2S+4H2O反应中,被氧化的元素是( )
| A、Cu | B、S | C、O | D、无法确定 |
下列说法正确的是( )
| A、H与D,16O与18O互为同位素;H216O、D216O、H218O、D218O互为同素异形体 |
| B、在SiO2晶体中,1个Si原子和2个O原子形成2个共价键 |
| C、HI的相对分子质量大于HF,所以HI的沸点高于HF |
| D、由ⅠA族和ⅥA族元素形成的原子个数比为1:1、电子总数为38的化合物,是含有共价键的离子型化合物 |
下列物质中既含有共价键又含有离子键的是( )
| A、C2H2 |
| B、Na2O |
| C、KOH |
| D、HClO |
下列化学用语或模型表示正确的是( )
A、氯化氢的电子式: |
B、甲烷的球棍模型: |
C、 名称为2-甲基-2-戊烯 名称为2-甲基-2-戊烯 |
D、三硝基甲苯的结构简式: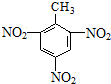 |