题目内容
雾霾严重影响人们的生活与健康.某地区的雾霾中可能含有如下可溶性无机离子:Na+、NH4+、Mg2+、Fe3+、SO42-、NO3-、CO32-、Cl-.某同学收集了该地区的雾霾,经必要的预处理后获得试样溶液,设计并完成了如下的实验:
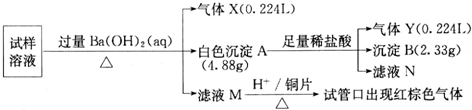
回答下列问题:
(1)气体X是 ,检验该气体通常使用的试剂是
(2)沉淀B是 ,在沉淀A中加入足量稀盐酸后,溶解的沉淀是 ;
(3)试样中肯定不存在的离子是 ,不能确定是否存在的离子是 ;
(4)滤液M在酸性条件下与铜片的反应中,还原产物是 .
(5)将实验中得到的气体Y全部通入10mL1.2mol?L-1的氢氧化钠溶液中,所得溶液中含有阴离子主要有 .

回答下列问题:
(1)气体X是
(2)沉淀B是
(3)试样中肯定不存在的离子是
(4)滤液M在酸性条件下与铜片的反应中,还原产物是
(5)将实验中得到的气体Y全部通入10mL1.2mol?L-1的氢氧化钠溶液中,所得溶液中含有阴离子主要有
考点:无机物的推断,物质的量的相关计算,常见离子的检验方法,物质的分离、提纯的基本方法选择与应用
专题:
分析:加入氢氧化钡,生成气体,说明含有NH4+,n(NH3)=
=0.01mol,生成沉淀4.88g,加入盐酸剩余沉淀2.33g,为硫酸钡,且生成0.224L气体,应为二氧化碳,则n(BaSO4)=
=0.01mol,n(BaCO3)=n(CO2)=
=0.01mol,则一定存在NH4+、SO42-、CO32-,则不存在Mg2+、Fe3+,由电荷守恒可知含有Na+,滤液加入酸,且加入铜片生成气体变为红棕色,说明含有NO3-,以此解答该题.
| 0.224L |
| 22.4L/mol |
| 2.33g |
| 233g/mol |
| 0.224L |
| 22.4L/mol |
解答:
解:加入氢氧化钡,生成气体,说明含有NH4+,n(NH3)=
=0.01mol,生成沉淀4.88g,加入盐酸剩余沉淀2.33g,为硫酸钡,且生成0.224L气体,应为二氧化碳,则n(BaSO4)=
=0.01mol,n(BaCO3)=n(CO2)=
=0.01mol,则一定存在NH4+、SO42-、CO32-,则不存在Mg2+、Fe3+,由电荷守恒可知含有Na+,滤液加入酸,且加入铜片生成气体变为红棕色,说明含有NO3-,
(1)由以上分析可知X为NH3,可用湿润的红色石蕊试纸检验,如有氨气,石蕊变蓝色,故答案为:NH3;湿润的红色石蕊试纸检验;
(2)沉淀B为BaSO4,在沉淀A中加入足量稀盐酸后,溶解的沉淀是BaCO3,故答案为:BaSO4;BaCO3;
(3)因存在CO32-,则一定不存在Mg2+、Fe3+,因Na+的物质的量不能确定,从电荷守恒的角度不能确定是否存在Cl-,则故答案为:Mg2+、Fe3+;Cl-;
(4)滤液M在酸性条件下与铜片的反应中,生成的气体在试管口被氧化生成红棕色的二氧化氮,则生成NO,故答案为:NO;
(5)n(CO2)=
=0.01mol,n(NaOH)=1.2mol/L×0.01L=0.012mol,首先发生CO2+2NaOH=Na2CO3+H2O,然后发生CO2+Na2CO3+H2O=2NaHNa2CO3,
反应后溶液中才能在的阴离子为HCO3-、CO32-,
故答案为:HCO3-、CO32-.
| 0.224L |
| 22.4L/mol |
| 2.33g |
| 233g/mol |
| 0.224L |
| 22.4L/mol |
(1)由以上分析可知X为NH3,可用湿润的红色石蕊试纸检验,如有氨气,石蕊变蓝色,故答案为:NH3;湿润的红色石蕊试纸检验;
(2)沉淀B为BaSO4,在沉淀A中加入足量稀盐酸后,溶解的沉淀是BaCO3,故答案为:BaSO4;BaCO3;
(3)因存在CO32-,则一定不存在Mg2+、Fe3+,因Na+的物质的量不能确定,从电荷守恒的角度不能确定是否存在Cl-,则故答案为:Mg2+、Fe3+;Cl-;
(4)滤液M在酸性条件下与铜片的反应中,生成的气体在试管口被氧化生成红棕色的二氧化氮,则生成NO,故答案为:NO;
(5)n(CO2)=
| 0.224L |
| 22.4L/mol |
反应后溶液中才能在的阴离子为HCO3-、CO32-,
故答案为:HCO3-、CO32-.
点评:本题考查较为综合,涉及物质的检验,侧重于学生的分析能力和计算能力的考查,注意把握反应的现象,结合反应的现象推断,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质在空气中不能稳定存在的是( )
| A、Fe(OH)2 |
| B、Fe(OH)3 |
| C、K3Fe(CN)6 |
| D、Cu(NH3)4SO4 |
如图所示是298K时,N2与H2反应过程中能量变化的曲线图,下列叙述正确的是( )
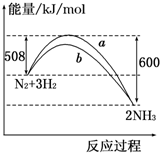

| A、该反应的热化学方程式为:N2+3H2?2NH3△H=-92 kJ/mol |
| B、a曲线是加入催化剂时的能量变化曲线 |
| C、加入催化剂,该化学反应的反应热改变 |
| D、在温度、体积一定的条件下,若通入2 mol N2和6 mol H2反应后放出的热量为Q kJ,则184>Q |
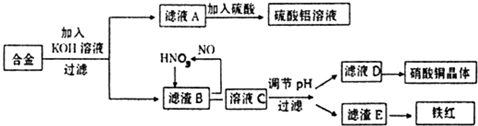
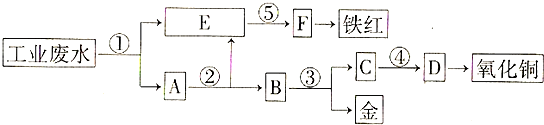
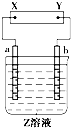 图中X、Y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无味气体放出,电解一段时间后,再加入相应的物质,溶液能与原来溶液完全一样.符合这一情况的是下表中的( )
图中X、Y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无味气体放出,电解一段时间后,再加入相应的物质,溶液能与原来溶液完全一样.符合这一情况的是下表中的( )