题目内容
1.下列说法不正确的是( )| A. | 煤是复杂的混合物,含有苯、甲苯、二甲苯等一系列重要的化工原料 | |
| B. | 石油分馏得到的汽油、煤油、柴油等各种沸点范围不同的混合物 | |
| C. | 通过石油裂化和裂解可以获得轻质油和重要化工原料(乙烯、丙烯等) | |
| D. | 天然气和沼气的主要成分是甲烷,它们都属于不可再生能源 |
分析 A、煤中不含芳香烃;
B、石油的分馏产物仍为混合物;
C、石油裂化的目的是为了获得轻质油;
D、沼气是可以再生的.
解答 解:A、煤中不含芳香烃,芳香烃可以通过煤的干馏生成,故A错误;
B、石油的分馏产物汽油、煤油和柴油等仍为多种烃的混合物,故均为固定的沸点,其沸点均在一定范围内,故B正确;
C、石油裂化的目的是为了获得轻质油,石油的裂解的目的是为了获得三烯,故C正确;
D、沼气是可以再生的,而天然气不能再生,但其主要成分均为甲烷,故D错误.
故选AD.
点评 本题考查了煤和石油的综合利用,难度不大,应注意的是煤中本不含苯及其同系物,是通过干馏生成的.

练习册系列答案
 目标测试系列答案
目标测试系列答案
相关题目
11.下列离子方程式书写正确的是( )
| A. | 碳酸钙与盐酸反应 CO32-+2H+=CO2↑+H2O | |
| B. | 铁钉放入硫酸铜溶液中 Fe+3Cu2+=2Fe3++3Cu | |
| C. | 氢氧化铜和硫酸反应 OH-+H+=H2O | |
| D. | 硫酸和氯化钡溶液反应 Ba2++SO42-=BaSO4↓ |
12.设NA表示阿伏加德罗常数的值,下列说法正确的是 ( )
| A. | 5.6 g Fe和足量的氯气完全反应失去电子数为0.3NA | |
| B. | 0.1molNa2O2固体与足量的H2O充分反应,转移0.2NA个电子 | |
| C. | 常温常压下,23 g NO2和N2O4的混合气体一定含有NA个氧原子 | |
| D. | 标况下,4.48L的水中含有H2O分子的数目为0.2NA |
9.将磁性氧化铁放入稀HNO3中可发生如下反应:3Fe3O4+28HNO3=9Fe(NO3)x+NO↑+14H2O,下列判断合理的是( )
| A. | Fe(NO3)x中的x为2 | |
| B. | 稀HNO3在反应中只表现氧化性 | |
| C. | 反应中每还原0.4 mol氧化剂,就有1.2 mol电子被转移 | |
| D. | 磁性氧化铁中的铁元素全部被氧化 |
16.向体积为2L的容器中加入1molN2和6molH2,合成氨.2分钟之后达到平衡,测得氮气为0.6mol.氢气的反应速率是( )
| A. | 0.1 mol•L-1•min-1 | B. | 0.2 mol•L-1•min-1 | ||
| C. | 0.3 mol•L-1•min-1 | D. | 0.6 mol•L-1•min-1 |
13.元素周期表中铋元素的数据如图,下列说法正确的是( )
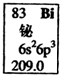

| A. | Bi元素的质量数是209 | |
| B. | Bi原子最外层有5个能量相同的电子 | |
| C. | Bi原子6p亚层有一个未成对电子 | |
| D. | Bi元素的相对原子质量是209.0 |
10.下列关于实验原理或操作的叙述中,不正确的是( )
| A. | 纸层析实验中,须将滤纸上的试样点浸入展开剂中 | |
| B. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度不一定要比水大 | |
| C. | 从碘水中提取单质碘时,不能用无水乙醇代替CCl4 | |
| D. | 分液操作时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出 |
11.二战期间,有支侦查小分队去炸毁德国法西斯的一座隐蔽且戒备森严的军火工厂,结果他们用十多只涂有化学药剂的老鼠完成了任务.据你推测这种化学药剂可能是( )
| A. | TNT | B. | 白磷的CS2溶液 | C. | 黑火药和甘油 | D. | KMnO4和H2SO4 |