题目内容
4.有关氯化钠叙述错误的是( )| A. | 是强电解质 | B. | 固体能导电 | ||
| C. | 电子式为: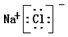 | D. | 25℃时,溶液的pH=7 |
分析 A、在水溶液中能完全电离的化合物为强电解质;
B、氯化钠固体中离子不能自由移动;
C、氯化钠是离子化合物,由钠离子和氯离子构成;
D、氯化钠是强酸强碱盐,在溶液中不水解.
解答 解:A、由于氯化钠在水溶液中能完全电离,故氯化钠为强电解质,故A正确;
B、有自由移动的离子或电子的物质才能导电,而氯化钠固体中离子不能自由移动,故不能导电,故B错误;
C、氯化钠是离子化合物,由钠离子和氯离子构成,故电子式为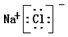 ,故C正确;
,故C正确;
D、氯化钠是强酸强碱的正盐,在溶液中不水解,故其溶液显中性,在25℃时,溶液的pH=7,故D正确.
故选B.
点评 本题借助氯化钠考查了强弱电解质的区别、物质导电的原因和盐类能否水解的原因,难度不大,应注意的是氯化钠固体不能导电,但是电解质.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
14.一定条件下,在密闭容器中充入一定量的X和Y发生可逆反应:X(g)+2Y(g)?3Z(g),达到平衡,测得Y的转化率为 37.5%,X的转化率为25%,则反应开始时,充入容器中的X和Y的物质的量之比为( )
| A. | 1:3 | B. | 3:1 | C. | 4:3 | D. | 3:4 |
15.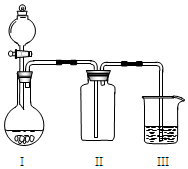 实验室中某些气体的制取、收集、尾气处理(或性质实验)装置如图所示,用此装置和表中提供的物质完成相关实验,其中合理的选项是( )
实验室中某些气体的制取、收集、尾气处理(或性质实验)装置如图所示,用此装置和表中提供的物质完成相关实验,其中合理的选项是( )
 实验室中某些气体的制取、收集、尾气处理(或性质实验)装置如图所示,用此装置和表中提供的物质完成相关实验,其中合理的选项是( )
实验室中某些气体的制取、收集、尾气处理(或性质实验)装置如图所示,用此装置和表中提供的物质完成相关实验,其中合理的选项是( )| 选项 | I中的物质 | II中收集的气体 | III中的物质 |
| A | Cu和浓硝酸 | NO | NaOH溶液 |
| B | 浓盐酸和高锰酸钾 | Cl2 | NaOH溶液 |
| C | 大理石和稀硫酸 | CO2 | 澄清石灰水 |
| D | 浓氨水和CaO | NH3 | 滴加酚酞的水 |
| A. | A | B. | B | C. | C | D. | D |
12.下列说法中不正确的是( )
| A. | 常温下,0.l mol•L-1CH3COOH溶液的pH=3,则CH3COOH的电离平衡常数约为10-5 | |
| B. | 常温下,pH=7的溶液中,K+、NH4+、NO3-、CH3COO-能大量共存 | |
| C. | 将NH3通入热的CuSO4溶液中能使Cu2+还原成Cu | |
| D. | 向Fe(OH)3胶体中逐滴加入盐酸,可观察到先生成红褐色沉淀,后沉淀溶解 |
19.次磷酸(H3PO2)是一种具有强还原性的一元弱酸,工业上常利用H3PO2和AgNO3溶液反应进行化学镀银,已知该反应中氧化剂与还原剂的物质的量之比为4:1,则下列说法中不正确的是( )
| A. | H3PO2中磷元素的化合价为+1 | |
| B. | H3PO2的电离方程式为H3PO2?H++H2 PO2- | |
| C. | H3PO2被AgNO3氧化成了H3PO4 | |
| D. | NaH2PO2、NaH2PO4、Na2HPO4均为酸式盐 |
9.有机物命名正确的是( )
| A. | CH2BrCH2Br 二溴乙烷 | B. | CH3OOCCH3甲酸乙酯 | ||
| C. | 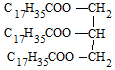 硬脂酸甘油脂 硬脂酸甘油脂 | D. | 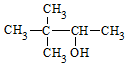 3,3-二甲基-2-丁醇 3,3-二甲基-2-丁醇 |
16.室温下,2H2(g)+O2(g)$\stackrel{点燃}{→}$2H2O(l)+566kJ.下列说法错误的是( )
| A. | H2→H+H的过程需要吸收热量 | |
| B. | 若生成2mol水蒸气,则放出的能量大于566 kJ | |
| C. | 2g氢气完全燃烧生成液态水所释放的能量为283kJ | |
| D. | 2mol氢气与1mol氧气的能量之和大于2mol液态水的能量 |
17.已知反应:CH3CHO(g)+O2(g)→X△H(未配平),X为下列何种物质时△H最小( )
| A. | CH3COOH(l) | B. | CH3COOH(g) | C. | CO(g)+H2O(l) | D. | CO2(g)+H2O(l) |
18.下列反应的离子方程式错误的是( )
| A. | AlCl3溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | Al(OH)3与过量NaOH溶液反应:Al(OH)3+OH-═AlO2-+2H2O | |
| C. | Al(OH)3与过量盐酸反应:Al(OH)3+H+═Al3++3H2O | |
| D. | AlCl3溶液中加入过量NaOH溶液:Al3++4OH-═AlO2-+2H2O |