题目内容
配制500mL0.5mol?L-1的NaOH溶液,试回答下列问题:
(1)计算:需要托盘天平称量NaOH固体的质量为
(2)某学生用托盘天平称量一个小烧杯的质量,称量前,把游码放在标尺的零刻度处,天平静止时,发现指针在分度盘的偏右位置,此时左边的托盘将 (填“高于”或者“低于”)右边的托盘.欲使天平平衡,所进行的操作为 .
(3)配制方法 设计五个操作步骤:
①向盛有NaOH的烧杯中加入200mL蒸馏水使其溶解,并冷却至室温.
②继续往容量瓶中加蒸馏水至液面接近刻度线1-2cm.
③将NaOH溶液沿玻璃棒注入500mL容量瓶中.
④在烧杯中加入少量的蒸馏水,小心洗涤2-3次,每次的洗涤液均移入容量瓶
⑤改用胶头滴管加蒸馏水至刻度线,加盖摇匀.
试将以上操作排出先后顺序 .
(4)某学生实际配制NaOH溶液的浓度为0.48mol?L-1,原因可能是 (填字母序号).
A、使用滤纸称量氢氧化钠固体
B、容量瓶中原来存有少量蒸馏水.
C、溶解后的烧杯未经多次洗涤
D、用胶头滴管定容时仰视刻度
(5)NaOH溶液长时间敞口放置在空气中,会部分变质为Na2CO3.取100mL0.5mol?L-1的NaOH的溶液,敞口放置一段时间去中和稀盐酸,消耗盐酸的量 0.05mol.(填“大于”“小于”或“等于”).
(1)计算:需要托盘天平称量NaOH固体的质量为
(2)某学生用托盘天平称量一个小烧杯的质量,称量前,把游码放在标尺的零刻度处,天平静止时,发现指针在分度盘的偏右位置,此时左边的托盘将
(3)配制方法 设计五个操作步骤:
①向盛有NaOH的烧杯中加入200mL蒸馏水使其溶解,并冷却至室温.
②继续往容量瓶中加蒸馏水至液面接近刻度线1-2cm.
③将NaOH溶液沿玻璃棒注入500mL容量瓶中.
④在烧杯中加入少量的蒸馏水,小心洗涤2-3次,每次的洗涤液均移入容量瓶
⑤改用胶头滴管加蒸馏水至刻度线,加盖摇匀.
试将以上操作排出先后顺序
(4)某学生实际配制NaOH溶液的浓度为0.48mol?L-1,原因可能是
A、使用滤纸称量氢氧化钠固体
B、容量瓶中原来存有少量蒸馏水.
C、溶解后的烧杯未经多次洗涤
D、用胶头滴管定容时仰视刻度
(5)NaOH溶液长时间敞口放置在空气中,会部分变质为Na2CO3.取100mL0.5mol?L-1的NaOH的溶液,敞口放置一段时间去中和稀盐酸,消耗盐酸的量
考点:溶液的配制
专题:实验题
分析:(1)依据n=C×V,m=n×M计算所需氢氧化钠的质量;
(2)依据天平的正确使用方法解答;
(3)配置一定物质的量浓度溶液的一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、装瓶等操作;
(4)依据C=
分析,操作对溶质的物质的量和溶液的体积的影响,凡是能够使n减小或者V增大的操作,都会使溶液的浓度偏低;
(5)氢氧化钠和碳酸钠都能够与盐酸反应均生成氯化钠,依据钠原子个数守恒计算解答.
(2)依据天平的正确使用方法解答;
(3)配置一定物质的量浓度溶液的一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、装瓶等操作;
(4)依据C=
| n |
| V |
(5)氢氧化钠和碳酸钠都能够与盐酸反应均生成氯化钠,依据钠原子个数守恒计算解答.
解答:
解:(1)配制500mL0.5mol?L-1的NaOH溶液,需要氢氧化钠的物质的量n=0.5L×0.5mol?L-1=0.25mol,其质量m=0.25mol×40g/mol=10.0g;
故答案为:10.0g;
(2)分度盘的指针偏右,说明右边重,左盘高于右盘.应将左边的横梁螺丝往外调以调节平衡;
故答案为:高于;将平衡螺母向左旋转,使之平衡;
(3)配置一定物质的量浓度溶液的一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、装瓶等;
故答案为:①③④②⑤;
(4)某学生实际配制NaOH溶液的浓度为0.48mol?L-1,依据C=
分析可知,操作使n减小或者V增大,都会导致所配溶液的浓度偏小;
A、使用滤纸称量氢氧化钠固体,氢氧化钠吸收空气中的水和二氧化碳,导致称取的氢氧化钠质量偏小,物质的量n偏小,溶液浓度偏小,故A正确;
B、容量瓶中原来存有少量蒸馏,对溶质的物质的量和溶液的体积都不会产生影响,溶液的浓度不变,故B错误;
C、溶解后的烧杯未经多次洗涤,导致溶质的物质的量n偏小,溶液的浓度偏小,故C正确;
D、用胶头滴管定容时仰视刻度,导致溶液的体积V偏大,溶液的浓度偏大,故D正确;
故选:ACD;
(5)氢氧化钠和碳酸钠都能够与盐酸反应均生成氯化钠,依据质量守恒定律,氢氧化钠中含的钠离子总是应等于盐酸中氯离子总是,所以n(HCl)=n(NaOH)=0.1L×0.5mol?L-1=0.05mol;
故答案为:等于.
故答案为:10.0g;
(2)分度盘的指针偏右,说明右边重,左盘高于右盘.应将左边的横梁螺丝往外调以调节平衡;
故答案为:高于;将平衡螺母向左旋转,使之平衡;
(3)配置一定物质的量浓度溶液的一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、装瓶等;
故答案为:①③④②⑤;
(4)某学生实际配制NaOH溶液的浓度为0.48mol?L-1,依据C=
| n |
| V |
A、使用滤纸称量氢氧化钠固体,氢氧化钠吸收空气中的水和二氧化碳,导致称取的氢氧化钠质量偏小,物质的量n偏小,溶液浓度偏小,故A正确;
B、容量瓶中原来存有少量蒸馏,对溶质的物质的量和溶液的体积都不会产生影响,溶液的浓度不变,故B错误;
C、溶解后的烧杯未经多次洗涤,导致溶质的物质的量n偏小,溶液的浓度偏小,故C正确;
D、用胶头滴管定容时仰视刻度,导致溶液的体积V偏大,溶液的浓度偏大,故D正确;
故选:ACD;
(5)氢氧化钠和碳酸钠都能够与盐酸反应均生成氯化钠,依据质量守恒定律,氢氧化钠中含的钠离子总是应等于盐酸中氯离子总是,所以n(HCl)=n(NaOH)=0.1L×0.5mol?L-1=0.05mol;
故答案为:等于.
点评:本题考查了一定物质的量浓度溶液的配置,明确物质的量浓度的含义和配置步骤是解题关键,注意质量守恒定律在计算中的应用.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
根据化学反应的实质是旧键断裂生成这一观点,下列变化不属于化学反应的是( )
| A、石墨转化为金刚石 |
| B、NaOH溶液与盐酸反应生成NaCl和H2O |
| C、NaCl熔化 |
| D、Na2O溶于水 |
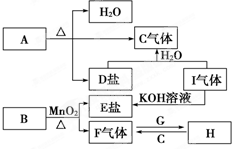 已知A、B、C、D、E、F、G、H、I九种物质,其中A、B、D、E焰色反应均为紫色(透过蓝色钴玻璃),G、F是单质,其余均为化合物,H是一种淡黄色固体,它们的转化关系如图所示.请回答:(提示:实验室制氧气可用氯酸钾与二氧化锰[作催化剂]混合加热制取)
已知A、B、C、D、E、F、G、H、I九种物质,其中A、B、D、E焰色反应均为紫色(透过蓝色钴玻璃),G、F是单质,其余均为化合物,H是一种淡黄色固体,它们的转化关系如图所示.请回答:(提示:实验室制氧气可用氯酸钾与二氧化锰[作催化剂]混合加热制取)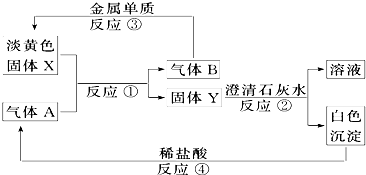
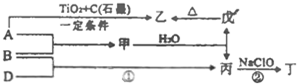 已知:A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物.其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,1mol丁分子中不同原子的数目比为1:2,且含有18mol电子;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用.各物质间的转化关系如图所示(某些条件已略去).
已知:A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物.其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,1mol丁分子中不同原子的数目比为1:2,且含有18mol电子;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用.各物质间的转化关系如图所示(某些条件已略去).