题目内容
11.下列有关物质结构的表述正确的是( )| A. | 氯化镁的分子式为MgCl2 | B. | 氮原子的轨道表达式为: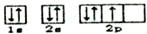 | ||
| C. | 硫原子的外围电子排布式为3s23p4 | D. | N2的结构式: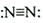 |
分析 A:氯化镁为离子晶体;
B、氮原子的电子排布式为1S22S22P3;
C、原子或离子核外电子排布属于基态排布应满足构造原理;
D、先写出氮气的电子式,将共用电子对用“-”表示即为结构式;
解答 解:A:氯化镁为离子晶体,不存在分子,应是氯化镁的化学式为MgCl2,故A错误;
B、氮原子的电子排布式为1S22S22P3,故轨道表达式为: ,故B正确;
,故B正确;
C、原子或离子核外电子排布属于基态排布应满足构造原理,S外围电子排布式应为3s23p4,故C正确;
D、氮气为共价单质,氮原子最外层有5个电子,其电子式为: ,则结构式为
,则结构式为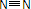 ,故D错误;
,故D错误;
故选BC.
点评 本题考查化学用语的使用,学生明确原子的最外层电子数及物质的类别、电子式的书写方法是解答本题的关键.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案
相关题目
19.含氮化合物是化学与工业中运用广泛的物质.
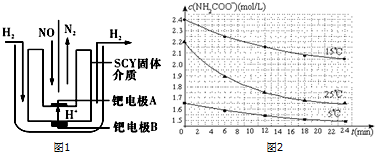
(1)该小组利用电解原理设计了如图1装置进行H2还原NO的实验(高质子导电性的SCY陶瓷(能传递H+)为介质,金属钯薄膜做电极).铂电极B是阳极,钯电极A的电极反应式为2NO+4H++4e-=N2+2H2O.
(2)若工业废水中的NO2-的浓度约为1.0×10-4 mol•L-1,取工业废水5mL 于试管中,滴加2滴0.1mol•L-1的硝酸银溶液,能否看到沉淀现象?试通过计算说明.(注:1mL溶液以20滴计;Ksp(AgNO2)=2×10-8)
(3)已知键能数据,H-H 436,S=S 255,H-S 339,单位kJ/mol.请计算热化学方程式2H2(g)+S2(g)=2H2S(g)的△H=-229KJ/mol
(4)将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g).
实验测得不同温度下的平衡数据列于下表:
?根据表中数据,列式计算25.0℃时的分解平衡常数:K=c(CO2)•c2(NH3)=[4.8×10-3×$\frac{2}{3}$]2×[4.8×10-3×$\frac{1}{3}$]=1.64×10-8.
?已知:NH2COONH4+2H2O?NH4HCO3+NH3•H2O.该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图2所示.根据图中信息,如何说明水解反应速率随温度升
高而增大:25.00C时反应物的起始浓度较小,但0-6min的平均反应速率(曲线的斜率)仍比15.00C的大.

(1)该小组利用电解原理设计了如图1装置进行H2还原NO的实验(高质子导电性的SCY陶瓷(能传递H+)为介质,金属钯薄膜做电极).铂电极B是阳极,钯电极A的电极反应式为2NO+4H++4e-=N2+2H2O.
(2)若工业废水中的NO2-的浓度约为1.0×10-4 mol•L-1,取工业废水5mL 于试管中,滴加2滴0.1mol•L-1的硝酸银溶液,能否看到沉淀现象?试通过计算说明.(注:1mL溶液以20滴计;Ksp(AgNO2)=2×10-8)
(3)已知键能数据,H-H 436,S=S 255,H-S 339,单位kJ/mol.请计算热化学方程式2H2(g)+S2(g)=2H2S(g)的△H=-229KJ/mol
(4)将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g).
实验测得不同温度下的平衡数据列于下表:
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡气体总浓度(×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
?已知:NH2COONH4+2H2O?NH4HCO3+NH3•H2O.该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图2所示.根据图中信息,如何说明水解反应速率随温度升
高而增大:25.00C时反应物的起始浓度较小,但0-6min的平均反应速率(曲线的斜率)仍比15.00C的大.
6.下列选项中符合如图关系的是( )
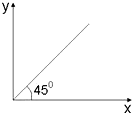

| A. | 第二周期的核电荷数和最高化合价之间的关系 | |
| B. | 烷烃中碳原子数(X)与氢原子数(Y)的关系 | |
| C. | 温度大于100℃时,CH4和C2H4的混合气体在氧气中充分燃烧,同温同压下燃烧前后参与反应的气体的体积之和(X)与生成物的气体体积之和(Y)的关系 | |
| D. | 燃烧一定质量C2H4与C3H6的混合气体,消耗O2的物质的量(Y)与C3H6的质量分数(X)的关系 |
16.碱金属元素具有相似的化学性质,是由于它们的原子具有相同的( )
| A. | 原子半径 | B. | 电子层数 | C. | 核外电子数 | D. | 最外层电子数 |
3.分子式为C9H11Cl芳香族化合物,其苯环上的一溴代物有两种,满足此条件的同分异构体有( )种.
| A. | 10 | B. | 11 | C. | 13 | D. | 14 |
20.能和对苯二甲酸发生缩聚反应的化合物是( )
| A. | 苯酚 | B. | 甲醛 | C. | 乙醇 | D. | 乙二醇 |
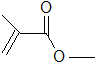
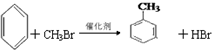 ;②C物质苯环上一卤代物只有两种.
;②C物质苯环上一卤代物只有两种.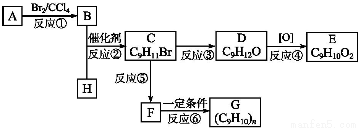
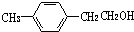 ,F的分子式C9H10.
,F的分子式C9H10.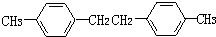 .
.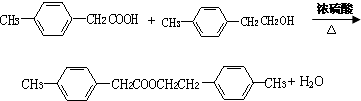 .
.