题目内容
4.某无色溶液,只可能由Na+、Ag+、Ba2+、Al3+、Cu2+、MnO4-、CO32-、Cl-中的若干种组成.为确定其成分,做如下实验:①取少量该溶液,加过量盐酸,有气体生成,得到甲溶液;②取少量甲溶液,向其中加硝酸酸化的硝酸银溶液,出现白色沉淀.请分析:
(1)该溶液一定没有的离子是Cu2+、MnO4-、Ag+、Ba2+、Al3+;
(2)一定有的离子Na+、CO32-;
(3)可能含有的离子是Cl-.
分析 无色溶液中不存在Cu2+、MnO4-,
①取少量该溶液,加过量盐酸,有气体生成,得到甲溶液,说明含有CO32-,则一定不存在Ag+、Ba2+、Al3+,由电荷守恒可知一定存在Na+;
②取少量甲溶液,向其中加硝酸酸化的硝酸银溶液,出现白色沉淀,说明生成AgCl,但由于加入盐酸,则不能说明是否含有Cl-,以此解答该题.
解答 解:(1)无色溶液中不存在Cu2+、MnO4-,取少量该溶液,加过量盐酸,有气体生成,得到甲溶液,说明含有CO32-,则一定不存在Ag+、Ba2+、Al3+,
故答案为:Cu2+、MnO4-、Ag+、Ba2+、Al3+;
(2)阳离子只有Na+,一定存在,生成气体,说明存在CO32-,故答案为:Na+、CO32-;
(3)取少量甲溶液,向其中加硝酸酸化的硝酸银溶液,出现白色沉淀,说明生成AgCl,但由于加入盐酸,则不能说明是否含有Cl-,故答案为:Cl-.
点评 本题考查离子检验,为高频考点,侧重考查学生的分析能力和实验能力,本题难度不大,做题时注意反应的现象,排除离子的相互干扰.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
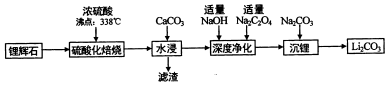
17.碳酸锂(相对分子质量74)广泛应用于化工、冶金等行业.工业上利用锂辉石(Li2Al2Si4Ox)制备碳酸锂的流程如图:
已知:碳酸锂的溶解度为((g/L)
请回答下列问题:
(1)锂辉(Li2Al2Si4Ox)可以用氧化物的形式表示其组成,形式为Li2O•Al2O3•4SiO2.
(2)硫酸化焙烧温度控制在250℃-300℃之间,主要原因是温度低于250℃,反应速率较慢,温度高于300℃,硫酸挥发较多.焙烧中硫酸用量控制在理论用最的l15%左右,硫酸加入过多的副作用是后续中还需要除去过量的硫酸,增加后续杂质的处理量、增加后续中和酸的负担.
(3)水浸时,加入CaCO3粉末充分反应后过滤,滤渣的主要成分除CaCO3外还有CaSO4、SiO2、Al(OH)3.
(4)“沉锂”的化学反应方程式为Na2CO3+Li2SO4=Li2CO3↓+Na2SO4.
(5)“沉锂”需要在95℃以上进行,主耍原因是温度越高,碳酸锂溶解度降低,可以增加产率.过滤碳酸锂所得母液中主要含有硫酸钠,还可能含有碳酸钠和碳酸锂.

已知:碳酸锂的溶解度为((g/L)
| 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
| Li2CO3 | 1.54 | 1.43 | 1.33 | 1.25 | 1.17 | 1.08 | 1.01 | 0.85 | 0.72 |
(1)锂辉(Li2Al2Si4Ox)可以用氧化物的形式表示其组成,形式为Li2O•Al2O3•4SiO2.
(2)硫酸化焙烧温度控制在250℃-300℃之间,主要原因是温度低于250℃,反应速率较慢,温度高于300℃,硫酸挥发较多.焙烧中硫酸用量控制在理论用最的l15%左右,硫酸加入过多的副作用是后续中还需要除去过量的硫酸,增加后续杂质的处理量、增加后续中和酸的负担.
(3)水浸时,加入CaCO3粉末充分反应后过滤,滤渣的主要成分除CaCO3外还有CaSO4、SiO2、Al(OH)3.
(4)“沉锂”的化学反应方程式为Na2CO3+Li2SO4=Li2CO3↓+Na2SO4.
(5)“沉锂”需要在95℃以上进行,主耍原因是温度越高,碳酸锂溶解度降低,可以增加产率.过滤碳酸锂所得母液中主要含有硫酸钠,还可能含有碳酸钠和碳酸锂.
4.铜粉放入稀硫酸溶液中,加热后无明显变化,但加入某盐一段时间后,发现铜粉质量减少,溶液呈蓝色,同时有气体逸出,该盐可能是( )
| A. | FeC13 | B. | Na2CO3 | C. | KNO3 | D. | FeSO4 |
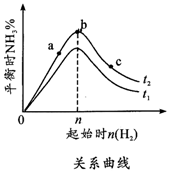 (1)在其他条件不变的情况下,起始氢气的物质的量[用n(H2)表示]对N2(g)+3H2(g) $?_{△}^{催化剂}$2NH3(g)△H<0反应的影响可表示成如图所示的规律(图中t表示温度,n表示物质的量).
(1)在其他条件不变的情况下,起始氢气的物质的量[用n(H2)表示]对N2(g)+3H2(g) $?_{△}^{催化剂}$2NH3(g)△H<0反应的影响可表示成如图所示的规律(图中t表示温度,n表示物质的量).