题目内容
将乙烯(C2H4),一氧化碳、氮气三种气体分别盛放在三个容器中,并保持三个容器内气体的温度和质量均相等,这三种气体对容器壁所施压强的大小关系是( )
| A、C2H4>CO>N2 |
| B、C2H4=CO=N2 |
| C、CO>C2H4>N2 |
| D、N2>C2H4>CO |
考点:阿伏加德罗定律及推论
专题:
分析:根据PV=nRT可知,温度相同的条件下,压强与气体的物质的量成正比,再根据n=
可知,容器内压强与气体的摩尔质量成反比,而三种气体的摩尔质量相等,则压强相等.
| m |
| M |
解答:
解:根据PV=nRT可知,温度相同的条件下,压强与气体的物质的量成正比,再根据n=
可知,容器内压强与气体的摩尔质量成反比,
乙烯、CO、氮气的摩尔质量都是28g/mol,
则三种气体对容器壁所施压强相等,
故选B.
| m |
| M |
乙烯、CO、氮气的摩尔质量都是28g/mol,
则三种气体对容器壁所施压强相等,
故选B.
点评:本题考查了阿伏伽德罗定律及其推论,题目难度中等,明确各个物理量之间的关系是解本题关键,注意公式的灵活转化,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
相关题目
当碳原子的核外电子排布由1s22s22p2转变为1s22s12p3时,下列说法正确的是( )
| A、碳原子由基态变为激发态 |
| B、碳原子由激发态变为基态 |
| C、该过程将产生发射光谱 |
| D、碳原子要向外界环境释放能量 |
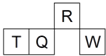 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断错误的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断错误的是( )| A、最简单气态氢化物的热稳定性:R>Q |
| B、最高价氧化物对应水化物的酸性:Q<W |
| C、T元素既显金属性又显非金属性 |
| D、原子半径:T>Q>R |
已知甲烷和一氧化碳混合气体对氢气的相对密度为11.6,则混合气体中甲烷与一氧化碳的体积比是( )
| A、1:1 | B、4:5 |
| C、2:3 | D、3:2 |
下列说法正确的是( )
| A、乙酸乙酯和淀粉均可水解生成乙醇 |
| B、溴乙烷、苯酚一定条件下都能与NaOH水溶液发生反应 |
| C、苯、乙烯都能使酸性KMnO4溶液褪色 |
| D、葡萄糖和蔗糖溶液都能发生银镜反应 |
新鲜水果、蔬菜、果汁中富含的维生素C具有明显的抗衰老作用,但易被空气氧化.某课外小组利用碘滴定法测某橙汁中维生素C的含量,用淀粉溶液作指示剂,其化学方程式为:下列说法正确的是( )
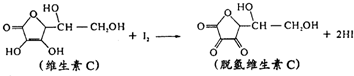

| A、上述反应为氧化反应 |
| B、脱氢维生素C的分子式为C6H6O6 |
| C、滴定时应剧烈振荡锥形瓶 |
| D、终点时溶液由蓝色恰好变无色 |

 经过反应也可制得化合物Ⅳ,则R在NaOH醇溶液中反应的化学方程式为:
经过反应也可制得化合物Ⅳ,则R在NaOH醇溶液中反应的化学方程式为: