题目内容
18.用锌片与1mol•L-1稀盐酸反应制取氢气,下列措施不能使反应速率增大的是( )| A. | 适当加热 | B. | 改用锌粉 | ||
| C. | 加入少量NaCl溶液 | D. | 加入少量1mol•L-1稀硫酸 |
分析 根据影响化学反应速率的因素分析,若增大反应速率,可以升高温度、增大锌的表面积、增大氢离子浓度等,而加入少量氯化钠溶液,导致原溶液中氢离子浓度减小,反应速率减小,据此进行解答.
解答 解:A.适当加热,会加快反应速率,故A不选;
B.锌片改为锌粉,增大了锌的接触面积,可以加快反应速率,故B不选;
C.加入少量氯化钠溶液,钠离子和氯离子不需要锌与氢离子的反应,而原溶液中氢离子浓度减小,导致反应速率减小,故C选;
D.加入1mol/L的稀硫酸,增大了溶液中氢离子浓度,从而加快了反应速率,故D不选;
故选C.
点评 本题考查了化学反应速率及其影响因素,题目难度不大,明确影响化学反应速率的因素为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.下列有关物质的量的说法中,正确的是( )
| A. | Fe的摩尔质量为56g | |
| B. | 常温常压下,71gCl2含有NA个Cl2分子 | |
| C. | 1mol O2在常温下的体积都为22.4L | |
| D. | 将1molNaCl晶体加入到1L水中,得到NaCl溶液的浓度就是1mol•L-1 |
9.在一个温度恒定且容积保持不变的容器中进行着如下反应:H2(g)+I2(g)?2HI(g),能说明该反应已达到平衡状态的是( )
| A. | 容器内${C_{({H_2})}}={C_{({I_2})}}={C_{(HI)}}$ | B. | 容器内的压强不再变化 | ||
| C. | 断裂1mol H-H的同时生成2mol H-I | D. | 容器内颜色不再变化 |
6.用酸性氢氧燃料电池电解饱和食盐水的装置如图所示 (a、b为石墨电极).下列说法中,正确的是( )
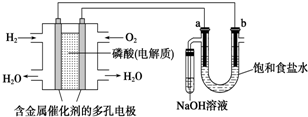

| A. | 电池工作时,正极反应式为:O2+2 H2O+4e-=4OH- | |
| B. | 忽略能量损耗,当电池中消耗0.1g H2时,b极周围会产生1.12L H2 | |
| C. | 电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极 | |
| D. | 电解时,a 电极周围首先放电的是Cl- |
13.下列各物质中互为同素异形体的是( )
| A. | 金刚石和石墨 | B. | CH3CH2OH与CH3OCH3 | ||
| C. | H2O和D2O | D. | 氘和氚 |
3.下列化学用语书写正确的是( )
| A. | 甲基的电子式: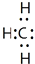 | B. | 2-丁烯的键线式: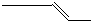 | ||
| C. | 丙烯的结构简式:CH2CHCH3 | D. | 乙醇的结构式: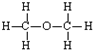 |
10.用NA表示阿伏加德罗常数.下列说法正确的是( )
| A. | 标准状况下,22.4 L 苯中含有的苯分子数是NA | |
| B. | 标准状况下,1mol氦气中含有的核外电子数为2NA | |
| C. | 常温常压下,15g乙烷分子数目为 NA | |
| D. | 常温常压下,0.10 mol•L-1CH3COOH溶液中含有的H+数小于0.1NA |
7.某有机物的核磁共振氢谱图如下,该有机物可能是( )
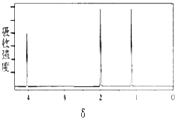

| A. | CH3-CH2-CH3 | B. | CH3CH2 CH2Br | C. | 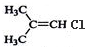 | D. | 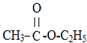 |
