题目内容
15.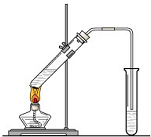 实验室我们可以用右图所示的装置制取乙酸乙酯.回答下列问题:
实验室我们可以用右图所示的装置制取乙酸乙酯.回答下列问题:(1)浓硫酸的作用是催化剂和吸水剂;
(2)制取乙酸乙酯的化学方程式CH3COOH+HOCH2CH3$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;
(3)下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的是CD.
A.单位时间里,生成1mol乙酸乙酯,同时生成1mol水
B.单位时间里,生成1mol乙醇,同时生成1mol乙酸
C.正反应的速率与逆反应的速率相等
D.混合物中各物质的浓度相等.
分析 (1)乙酸与乙醇需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动;
(2)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应为可逆反应;
(3)当可逆反应达到平衡状态时,正逆反应速率相等(同种物质)或正逆反应速率等于化学计量数之比(不同物质),各物质的浓度、质量、体积分数以及百分含量不变,以及由此衍生的一些量也不发生变化.
解答 解:(1)酸与乙醇需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动.故浓硫酸的作用为催化剂,吸水剂.
故答案为:催化剂、吸水剂;
(2)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,同时该反应可逆,反应的化学方程式为:CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O.
故答案为:CH3COOH+HOCH2CH3$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;
(3)A.单位时间里,生成1mol乙酸乙酯,同时生成1mol水,都表示正反应速率,不能说明到达平衡状态,故A错误;
B.单位时间里,生成1mol乙醇,同时消耗1mol乙酸,都表示正反应速率,不能说明到达平衡状态,故B错误;
C.正反应的速率与逆反应的速率相等,说明到达平衡状态,故C正确;
D.混合物中各物质的浓度不再变化,反应到达平衡状态,故D正确.
故答案为:CD.
点评 本题考查乙酸乙酯的制备,注意实验混合液的配制、饱和碳酸钠溶液的作用以及酯化反应的机理,题目难度中等.

练习册系列答案
相关题目
2.实验室用H2SO4滴定氨水,选用的指示剂是( )
| A. | 甲基橙 | B. | 石蕊 | C. | 酚酞 | D. | 任选一种均可以 |
3.下列说法正确的是( )
| A. | 减小反应物浓度,可减小单位体积内活化分子的百分数,从而使有效碰撞次数减少 | |
| B. | 对于有气体参加的化学反应,若减小压强(即扩大反应容器的体积),可减小活化分子的百分数,从而使反应速率减小 | |
| C. | 改变条件能使化学反应速率增大的主要原因是增大了反应物分子中活化分子的有效碰撞几率 | |
| D. | 能量高的分子一定能发生有效碰撞 |
4.对如下反应:CO(气)+2H2(气)?CH3OH(气)(正反应为放热反应),为提高单位时间内CH3OH的产量,工厂应控制的反应条件是( )
| A. | 高温、低压 | B. | 适宜的温度、高压、催化剂 | ||
| C. | 低温、低压 | D. | 低温、高压、催化剂 |
5.下列物质存放在烧杯中一段时间后,质量变大且变质的是( )
①浓盐酸 ②浓硫酸 ③烧碱 ④食盐 ⑤生石灰 ⑥稀硫酸.
①浓盐酸 ②浓硫酸 ③烧碱 ④食盐 ⑤生石灰 ⑥稀硫酸.
| A. | ①⑥ | B. | ②③⑤ | C. | ③⑤ | D. | ②③④ |
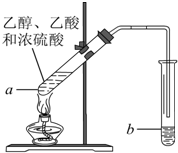 红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯.在实验室也可以用如图所示的装置制取乙酸乙酯,请回答下列问题.
红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯.在实验室也可以用如图所示的装置制取乙酸乙酯,请回答下列问题.