题目内容
下列说法正确的是( )
| A、金属钠和其他碱金属都可保存在煤油中 |
| B、湿法冶炼是指金属在溶液中发生的置换反应,如金属钠置换出硫酸铜溶液中的铜 |
| C、用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 |
| D、制备AlCl3、MgCl2、FeCl3均不能采用将溶液直接蒸干的方法 |
考点:钠的化学性质,盐类水解的应用,焰色反应
专题:元素及其化合物,化学应用
分析:A.Li不能保存在煤油中;
B.钠和硫酸铜溶液中水先发生反应生成NaOH,然后NaOH再和硫酸铜发生复分解反应;
C.用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液可能是钠盐溶液或氢氧化钠溶液;
D.AlCl3、MgCl2、FeCl3都易发生水解且HCl具有挥发性.
B.钠和硫酸铜溶液中水先发生反应生成NaOH,然后NaOH再和硫酸铜发生复分解反应;
C.用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液可能是钠盐溶液或氢氧化钠溶液;
D.AlCl3、MgCl2、FeCl3都易发生水解且HCl具有挥发性.
解答:
解:A.Li的密度小于煤油,所以Li保存在煤油中不能隔绝空气和水,故A错误;
B.钠和硫酸铜溶液中水先发生反应生成NaOH,然后NaOH再和硫酸铜发生复分解反应,反应方程式为2Na+2H2O=2NaOH+H2↑、CuSO4+2NaOH=Cu(OH)2↓+Na2SO4,所以不能置换出Cu,故B错误;
C.用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,说明该溶液中含有钠元素,则该溶液可能是钠盐溶液或氢氧化钠溶液,故C错误;
D.AlCl3、MgCl2、FeCl3都易发生水解生成氢氧化物且有HCl生成,HCl具有挥发性,随着反应的进行,促进HCl挥发,从而促进水解,则最终得不到AlCl3、MgCl2、FeCl3,故D正确;
故选D.
B.钠和硫酸铜溶液中水先发生反应生成NaOH,然后NaOH再和硫酸铜发生复分解反应,反应方程式为2Na+2H2O=2NaOH+H2↑、CuSO4+2NaOH=Cu(OH)2↓+Na2SO4,所以不能置换出Cu,故B错误;
C.用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,说明该溶液中含有钠元素,则该溶液可能是钠盐溶液或氢氧化钠溶液,故C错误;
D.AlCl3、MgCl2、FeCl3都易发生水解生成氢氧化物且有HCl生成,HCl具有挥发性,随着反应的进行,促进HCl挥发,从而促进水解,则最终得不到AlCl3、MgCl2、FeCl3,故D正确;
故选D.
点评:本题考查了物质的保存、焰色反应、盐类水解的呢过知识点,明确物质的性质是解本题关键,根据钠的性质、盐的特点来分析解答即可,题目难度不大.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
氢有H、D、T三种同位素,氯有35Cl、37Cl两种同位素,则形成的氯化氢分子的种类有( )
| A、2 | B、5 | C、6 | D、9 |
下列说法中不正确的是( )
| A、化学变化过程是原子的重新组合过程 |
| B、化学反应可分为吸热反应和放热反应 |
| C、化学反应中能量变化的多少与其反应物的质量有关 |
| D、化学变化中的能量变化都是以热能形式表现出来的 |
以下物质间的每步转化通过一步反应能实现的是( )
| A、Al-Al2O3-Al(OH)3-NaAlO2 |
| B、Na-Na2O2-Na2CO3-NaOH |
| C、S-SO3-H2SO4-MgSO4 |
| D、Fe-FeO-Fe(OH)2-Fe(OH)3 |
下列操作错误的是( )
| A、提取溶解在水中的少量碘:加入CCl4,振荡、静置分层后,从分液漏斗下端放出I2的CCl4溶液 |
| B、把1 mL饱和FeCl3溶液逐滴加入到20 mL温水中,边加边振荡,并加热到沸腾可得Fe(OH)3胶体 |
| C、除去CO气体中少量的CO2:通过盛有NaOH溶液的洗气瓶 |
| D、某溶液中滴入稀盐酸酸化的氯化钡溶液,生成白色沉淀,说明原溶液中有SO42- |
某物质在酸性条件下可以发生水解反应生成A、B两种物质,且A和B相对分子质量相同.则该有机物可能是( )
| A、甲酸乙酯(HCOOC2H5) |
| B、硬脂酸甘油酯: |
| C、葡萄糖 (C6H12O6) |
| D、淀粉[(C6H10O5)n] |
下面4组物质中,能发生反应且既属于离子反应又属于氧化还原反应的是( )
| A、硫酸钠溶液与氯化钡溶液 |
| B、铝片与硝酸汞溶液 |
| C、稀硫酸与铜片 |
| D、硝酸钠溶液与氯化钾溶液 |
下列有关油脂的说法错误的是( )
| A、油脂的主要成分是高级脂肪酸的甘油酯,属于酯类 |
| B、天然油脂大多数是由混甘油酯构成的混合物 |
| C、油脂的水解反应叫做皂化反应 |
| D、油脂里饱和烃基的相对含量越大,熔点越高 |
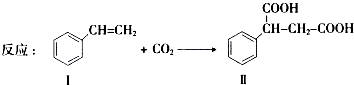
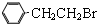 通过消去反应制备Ⅰ的化学方程式为
通过消去反应制备Ⅰ的化学方程式为