题目内容
18.CuS 与HNO3反应后的产物为CuSO4、NO和H2O,下列说法正确的是( )| A. | 氧化剂与还原剂的物质的量之比为 8﹕3 | |
| B. | 氧化剂与还原剂的物质的量之比为 3﹕8 | |
| C. | 若有 1 mol NO 气体生成,转移的电子总数为 6 mol | |
| D. | 反应的离子方程式为 CuS+2H++2NO3-═Cu2++2NO↑+SO42-+H2O |
分析 CuS 与HNO3反应后的产物为CuSO4、NO和H2O,反应方程式为:3CuS+8HNO3=3CuSO4+8NO↑+4H2O,CuS是还原剂,硝酸是氧化剂,由此分析解答.
解答 解:CuS 与HNO3反应后的产物为CuSO4、NO和H2O,反应方程式为:3CuS+8HNO3=3CuSO4+8NO↑+4H2O,CuS是还原剂,硝酸是氧化剂,
A、氧化剂硝酸与还原剂CuS 的物质的量之比为 8﹕3,故A正确;
B、氧化剂硝酸与还原剂CuS 的物质的量之比为 8﹕3,而不是3﹕8,故B错误;
C、8mol转移24mol的电子,则 1 mol NO 气体生成,转移的电子总数为3 mol,故C错误;
D、反应的离子方程式为 3CuS+8H++8NO3-═3Cu2++8NO↑+3SO42-+4H2O,故D错误;
故选A.
点评 本题考查氧化还原反应,明确元素化合价是解本题关键,注意该反应中化合价变化是解题的关键所在,为易错点.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
8.短周期主族元素X、Y、Z、W、R的原子序数依次增大,其中前四种元素原子的最外层电子数之和为14.X是周期表中原子半径最小的元素,Z是短周期中金属性最强的元素,Y与W同主族.下列说法不正确的是( )
| A. | 原子半径:X<W<Z | |
| B. | 最高价氧化物对应水化物的酸性:W>R | |
| C. | R在周期表中的位置为第三周期ⅦA族 | |
| D. | 简单气态氢化物的热稳定性:Y>W |
9.常温下,将等质量的铜片、银片、铁片、铝片分别置于四个小烧杯中,然后分别加入足量的浓硝酸,放出NO2气体最多的是( )
| A. | 铜片 | B. | 银片 | C. | 铁片 | D. | 铝片 |
6.常温下,下列溶液可以用铝制器皿盛放的是( )
| A. | 浓盐酸 | B. | 氢氧化钠 | C. | 浓硝酸 | D. | 硫酸铜 |
13.下列各组物质充分反应后,再滴入 KSCN 溶液,显红色的是( )
| A. | 足量氯水与 FeCl2 溶液 | B. | 足量铁与稀盐酸 | ||
| C. | 足量铁粉与CuCl2 溶液 | D. | 足量铁粉与 FeCl3 溶液 |
3.下列物质属于弱电解质的是( )
| A. | 氯化钠 | B. | 稀盐酸 | C. | 醋酸 | D. | 酒精 |
10.质量为2.3g含有一种金属杂质的金属钠,放入足量的稀硫酸中反应,得到氢气0.09g,则所含的金属杂质可能是( )
| A. | K | B. | Mg | C. | Al | D. | Cu |
7.下列变化中,需加入还原剂的是( )
| A. | SO2→SO3 | B. | HCl→NaCl | C. | KI→I2 | D. | Fe2O3→Fe |
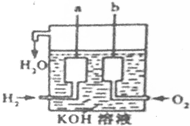 (1)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如图所示:a、b两个电极均由多孔的碳块组成.写出b极的电极反应方程式.工作时电池负极区的pH减小(填“增大”、“减小”或“不变”).
(1)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如图所示:a、b两个电极均由多孔的碳块组成.写出b极的电极反应方程式.工作时电池负极区的pH减小(填“增大”、“减小”或“不变”).