题目内容
15.结合元素周期律,判断下列说法中正确的是( )| A. | 核外电子层数越多的微粒半径一定较大 | |
| B. | 由5R-+RO-+6H+=3R+3H2O 判断,R元素可能是第ⅤA族元素 | |
| C. | 元素周期表对于生产和科研具有重要的指导意义,如半导体材料通常位于过渡元素区 | |
| D. | 既有非金属元素简单阴离子,又有非金属元素简单阳离子 |
分析 A.如不是同主族,则电子层多的,微粒半径不一定大;
B.由R-可确定R最外层有7个电子;
C.半导体材料位于金属和非金属的分界线;
D.非金属元素得电子可形成简单阴离子,金属元素失电子可形成简单阳离子.
解答 解:A.如不是同主族,则电子层多的,微粒半径不一定大,如Cl比Li多一个电子层,但原子半径比Li小,故A错误;
B.由R-可确定R最外层有7个电子,应为ⅦA族元素,故B错误;
C.半导体材料位于金属和非金属的分界线,故C错误;
D.非金属元素得电子可形成简单阴离子,金属元素失电子可形成简单阳离子,则既有非金属元素简单阴离子,又有非金属元素简单阳离子,故D正确.
故选D.
点评 本题考查了原子结构与元素周期表的关系,为高频考点,侧重考查学生的分析能力,题目难度中等,正确推断各元素为解答关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.下列各项中:①土地沙漠化②酸雨③水资源危机④臭氧层空洞⑤沙尘暴,其中属于因人类生产、生活对环境造成破坏的是( )
| A. | 只有①②⑤ | B. | 只有①②③⑤ | C. | 只有②③④ | D. | 全部 |
3.基态硅原子的最外能层的各能级中,电子排布的方式正确的是( )
| A. | 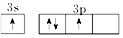 | B. | 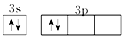 | C. | 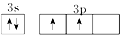 | D. |  |
10.四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径在短周期主族元素原子中最大,Y的核外电子数是W的2倍且同主族.下列说法不正确的是( )
| A. | 简单离子半径:X<W<Z | |
| B. | W、X、Y元素形成的盐溶于水,溶液一定呈中性 | |
| C. | W与X形成的常见化合物中阴、阳离子个数比均为1:2 | |
| D. | 1 mol Z 的单质与足量的NaOH溶液反应转移电子数1 NA |
20.下列根据实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 取等物质的量的两种金属单质X、Y,分别与足量的盐酸反应 | X产生氢气的体积比Y多 | 金属性:X>Y |
| B | 用玻璃棒蘸取浓硫酸点到蓝色石蕊试纸上 | 试纸变黑 | 浓硫酸具有脱水性 |
| C | 将蘸有浓氨水的玻璃棒置于某无机酸浓溶液的试剂瓶口 | 有大量白烟 | 该无机酸一定为盐酸 |
| D | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有变质 |
| A. | A | B. | B | C. | C | D. | D |
7. 已知X、Y、Z、W为短周期元素,X的一种核素的质子数为8;Y和Ne原子的原子核外电子数相差1;Z的单质是一种常见的半导体材料;W的非金属性在同周期元素中最强.其原子半径随原子序数的变化如图所示.下列说法不正确的是( )
已知X、Y、Z、W为短周期元素,X的一种核素的质子数为8;Y和Ne原子的原子核外电子数相差1;Z的单质是一种常见的半导体材料;W的非金属性在同周期元素中最强.其原子半径随原子序数的变化如图所示.下列说法不正确的是( )
 已知X、Y、Z、W为短周期元素,X的一种核素的质子数为8;Y和Ne原子的原子核外电子数相差1;Z的单质是一种常见的半导体材料;W的非金属性在同周期元素中最强.其原子半径随原子序数的变化如图所示.下列说法不正确的是( )
已知X、Y、Z、W为短周期元素,X的一种核素的质子数为8;Y和Ne原子的原子核外电子数相差1;Z的单质是一种常见的半导体材料;W的非金属性在同周期元素中最强.其原子半径随原子序数的变化如图所示.下列说法不正确的是( )| A. | ZX2为酸性氧化物,只能与碱溶液反应 | |
| B. | 简单氢化物的热稳定性:Z<W | |
| C. | 化合物YWX中既含离子键,又含共价键 | |
| D. | W的最高价氧化物对应的水化物为强酸 |
4.一定温度下,反应N2(g)+O2(g)?2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是
( )
( )
| A. | 恒容充入N2 | B. | 缩小体积使压强增大 | ||
| C. | 恒容充入氦气 | D. | 恒压充入氦气 |
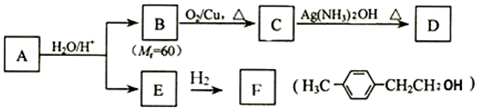
 .
. (其中一种).
(其中一种). )的合成路线.
)的合成路线.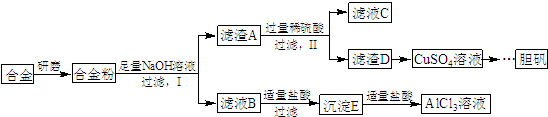
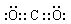 ,写出更改试剂(气体过量)后生成沉淀E所发生反应的离子方程式:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-.
,写出更改试剂(气体过量)后生成沉淀E所发生反应的离子方程式:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-.