题目内容
测定分子量的常用方法之一是凝固点下降法.例如水是常用的溶剂,当水中溶解了某种不挥发的溶质时,水的凝固点(即冰点)即会下降,海水在0℃时不会结冰就是这个原因.凝固点下降的程度与溶质的分子数有关,而与溶质是何种物质无关.当溶剂的量确定时,凝固点的降低值与溶质的分子数成正比.已知10.0g樟脑中溶解0.412g萘,凝固点下降了13℃.某种由C、H、O组成的有机物2.30g溶于15.6g樟脑中,凝固点下降了49.5℃.如果把3.667g该有机物完全燃烧,生成 9.236g CO2和1.634g H2O,求该物质的分子式(已知萘的相对分子质量为:128,相对原子质量:H:1 C:12 O:16)
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:根据题干信息可知,樟脑中溶解的该有机物的物质的量与溶解的萘的物质的量相等,根据“10.0g樟脑中溶解0.412g萘,凝固点下降了13℃”计算出15.6g樟脑中,凝固点下降了49.5℃溶解的该有机物的物质的量,即2.30g该有机物的物质的量,从而得出该有机物的摩尔质量;根据n=
计算出3.66g该有机物的物质的量及燃烧生成二氧化碳、水的质量计算出C、H的物质的量,然后可以确定该有机物分子中含有的C、H原子数,最后根据摩尔质量确定其分子式.
| m |
| M |
解答:
解:0.412g萘的物质的量为:n=
=
≈0.00322mol,10.0g樟脑中溶解0.00322mol萘,也能够溶解相同物质的量的该有机物,
即10.0g樟脑中溶解0.00322mol该有机物时温度降低了13℃,
则15.6g樟脑中溶解该有机物温度降低13℃时,溶解的该有机物的物质的量为:0.00322mol×
≈0.005mol,
2.30g溶于15.6g樟脑中,凝固点下降了49.5℃,则溶解的该有机物的物质的量为:0.005mol×
≈0.019mol,
该有机物的摩尔质量为:M=
=
=121g/mol,
3.667g该有机物的物质的量为:n=
≈0.0303mol,
9.236g CO2的物质的量为:
≈0.21mol,则3.667g该有机物中:n(C)=0.21mol,
1.634g H2O的物质的量为:
≈0.0908mol,则n(H)=0.0908mol×2=0.1816mol,
该有机物分子中含有C、H原子数为:N(C)=
≈712、N(H)=
≈6,
则该有机物分子中含有氧原子数目为:
≈2,
该有机物 分子式为:C7H6O2,
答:该有机物分子式为C7H6O2.
| 0.412g |
| 128g/mol |
| 0.412 |
| 128 |
即10.0g樟脑中溶解0.00322mol该有机物时温度降低了13℃,
则15.6g樟脑中溶解该有机物温度降低13℃时,溶解的该有机物的物质的量为:0.00322mol×
| 15.6g |
| 10.0g |
2.30g溶于15.6g樟脑中,凝固点下降了49.5℃,则溶解的该有机物的物质的量为:0.005mol×
| 49.5℃ |
| 13℃ |
该有机物的摩尔质量为:M=
| m |
| n |
| 2.3g |
| 0.019mol |
3.667g该有机物的物质的量为:n=
| 3.667g |
| 121g/mol |
9.236g CO2的物质的量为:
| 9.236g |
| 44g/mol |
1.634g H2O的物质的量为:
| 1.6344g |
| 18g/mol |
该有机物分子中含有C、H原子数为:N(C)=
| 0.21mol |
| 0.0303mol |
| 0.1816mol |
| 0.0303mol |
则该有机物分子中含有氧原子数目为:
| 121-12×7-1×6 |
| 16 |
该有机物 分子式为:C7H6O2,
答:该有机物分子式为C7H6O2.
点评:本题考查了有机物分子式的确定,题目难度较大,注意理解题干信息从而确定该有机物的摩尔质量为解答本题的关键,试题培养了学生的分析、理解能力及化学计算能力.

练习册系列答案
相关题目
下列实验操作中不正确的是( )
| A、分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口处 |
| C、过滤时,若过滤速度太慢,可以拿玻璃棒搅拌漏斗中固体,加快过滤速度 |
| D、焰色反应实验时,可以用洁净的铁丝直接蘸取所测试剂的固体粉末,置于煤气灯火焰上灼烧 |
汶川“5?12”大地震震惊全球,一些化工厂受地震影响相继发生过氨气泄漏事故和重大液氯泄漏事故,幸好部队抢险及时,避免了人民生命财产的损失.下列有关氯气和氨气的说法正确的是( )
| A、氯气和氨气都是由极性键构成的分子 |
| B、氯气和氨气都是无色、密度比空气大的有毒气体 |
| C、氯气和氨气都是易液化的气体 |
| D、氯气和氨气分子中所有原子都满足最外层为8电子结构 |
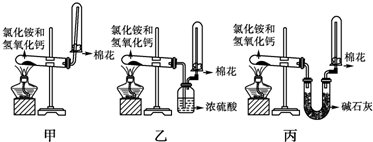
用下列实验装置完成对应的实验(部分仪器已省略),操作正确并能达到实验目的是( )
A、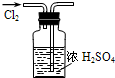 干燥Cl2 |
B、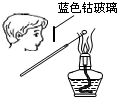 检验K2CO3中的K+ |
C、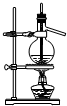 石油的蒸馏 |
D、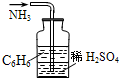 吸收NH3 |
下列关于能量的变化及反应热的说法中正确的是( )
| A、任何化学反应都有反应热 |
| B、有些化学键断裂时吸收能量,有些化学键断裂时放出能量 |
| C、新化学键的形成不一定放出能量 |
| D、有热量变化的反应一定有化学键的断裂与形成 |
 感光高分子材料是制作大规模集成电路不可缺少的材料,感光高分子在曝光时会发生二聚反应,生成不溶性的交联高分子硬化膜,未感光部分可用溶剂或其它药品洗去.常用的感光高分子有聚肉桂酸乙烯酯,它的结构简式如右图,它感光后形成二聚交联高分子.请据此回答下列问题:
感光高分子材料是制作大规模集成电路不可缺少的材料,感光高分子在曝光时会发生二聚反应,生成不溶性的交联高分子硬化膜,未感光部分可用溶剂或其它药品洗去.常用的感光高分子有聚肉桂酸乙烯酯,它的结构简式如右图,它感光后形成二聚交联高分子.请据此回答下列问题: 和
和 外还有两种,请写出其结构简式:
外还有两种,请写出其结构简式: