题目内容
关于晶体的下列说法正确的是( )
| A、化学键都具有饱和性和方向性 |
| B、晶体中只要有阴离子,就一定有阳离子 |
| C、氢键具有方向性和饱和性,也属于一种化学键 |
| D、金属键由于无法描述其键长、键角,故不属于化学键 |
考点:不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:A.离子键通过阴阳离子之间的相互作用形成,离子键没有方向性和饱和性,而共价键有方向性和饱和性;
B.晶体中只要有阴离子,就一定有阳离子中和阴离子的电性;
C.氢键具有方向性和饱和性,但不属于化学键;
D.金属键由于无法描述其键长、键角,但属于化学键;
B.晶体中只要有阴离子,就一定有阳离子中和阴离子的电性;
C.氢键具有方向性和饱和性,但不属于化学键;
D.金属键由于无法描述其键长、键角,但属于化学键;
解答:
解:A.离子键通过阴阳离子之间的相互作用形成,离子键没有方向性和饱和性,共价键是原子之间通过共用电子对形成,所以共价键有方向性和饱和性,故A错误;
B.在晶体中有阴离子,根据物质呈电中性,有阴离子,那么一定有阳离子中和阴离子的电性,故B正确;
C.氢键饱和性,是指一个氢原子只能和一个氧(氟,氮)原子,形成氢键,而不能同时和多个原子形成氢键;方向性,是指氢键是有一定键角,但氢键属于分子间作用力,不属于化学键,故C错误;
D.金属键是金属阳离子和自由电子这两种带异性电荷的微粒间的强烈相互作用,金属键没有方向性和饱和性,无法描述其键长、键角,但属于化学键,故D错误;
故选B.
B.在晶体中有阴离子,根据物质呈电中性,有阴离子,那么一定有阳离子中和阴离子的电性,故B正确;
C.氢键饱和性,是指一个氢原子只能和一个氧(氟,氮)原子,形成氢键,而不能同时和多个原子形成氢键;方向性,是指氢键是有一定键角,但氢键属于分子间作用力,不属于化学键,故C错误;
D.金属键是金属阳离子和自由电子这两种带异性电荷的微粒间的强烈相互作用,金属键没有方向性和饱和性,无法描述其键长、键角,但属于化学键,故D错误;
故选B.
点评:本题考查化学键知识,熟悉化学键种类并掌握其特征是解答的关键,题目概念性强,注意集中化学键的区别和联系,注意氢键不属于化学键,题目难度不大.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
各可逆反应达平衡后,改变反应条件,其变化趋势正确的是( )
A、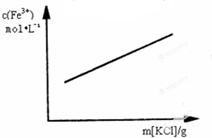 FeCl3+3KSCN?Fe(SCN)3+KCl(忽略液体体积变化) | ||
B、 2NO+O2?2NO2△H<0 | ||
C、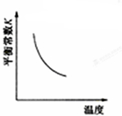 NO(g)+CO(g)?
| ||
D、 A2(g)+3B2(g)?2AB3(g)△H=-373.4KJ?mol-1 |
在可逆反应:X(g)+2Y(g)?2Z(g)(△H>0),为了有利于Z的生成,应采用的反应条件是( )
| A、高温高压 | B、高温低压 |
| C、低温高压 | D、低温低压 |
下列说法正确的是( )
| A、原子的电子层数越多,原子半径越大 |
| B、同族元素相差的原子序数可能为16、26、36、46 |
| C、ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物 |
| D、卤族元素的单质均有氧化性,最高正价都是+7 |
下列化学(或离子)方程式正确的是( )
| A、乙酸与碳酸钠溶液反应:2H++CO32-═CO2↑+H2O | |||
B、C6H6+HNO3
| |||
| C、亚硫酸的电离方程式:H2SO3?2H++SO32- | |||
| D、醋酸溶液与新制氢氧化铜反应:CH3COOH+OH-→CH3COO-+H2O |
下列说法正确的是( )
| A、将AlCl3溶液、Na2SO3溶液蒸干并灼烧可分别得到Al2O3、Na2SO3 | ||
| B、在溶液的稀释过程中,离子浓度有的可能增大,有的可能减小,有的可能不变 | ||
C、0.1 mol/L CH3COOH溶液在稀释过程中
| ||
| D、已知MgCO3的Ksp═6.82×10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+)═c(CO32-),且c(Mg2+)?c(CO32-)═6.82×10-6 |
 将CH4和Cl2按体积比1:2混合充入大试管中,将此试管倒立在盛Na2SiO3溶液的水槽里,放在光亮处,如图所示下列描述正确的是( )
将CH4和Cl2按体积比1:2混合充入大试管中,将此试管倒立在盛Na2SiO3溶液的水槽里,放在光亮处,如图所示下列描述正确的是( )| A、由于Cl2不足,生物中不含有CHCl3、CCl4 |
| B、CH4和Cl2取代的产物全部都是极性分子 |
| C、水槽底部出现白色沉淀 |
| D、最终试管内全部充满溶液 |
下列分子中,电子总数最少的是( )
| A、H2S |
| B、O2 |
| C、CO |
| D、NO |
除去CuSO4溶液中含有的Fe2(SO4)3杂质,最佳的方法是加入( )
| A、CuO |
| B、H2O2 |
| C、NH3?H2O |
| D、NaOH |