题目内容
下列说法中正确的是( )
| A、将322 g Na2SO4?10H2O溶于1 L水中,所得溶液的物质的量浓度为1 mol/L |
| B、将1 L 2 mol/L H2SO4溶液加水稀释到2 L,所得溶液的物质的量浓度为1 mol/L |
| C、将1 L 18.4 mol/L的H2SO4溶液加入到1 L水中,所得溶液的物质的量浓度为9.2 mol/L |
| D、将336 mL HCl气体溶于水,配成300 mL溶液,所得溶液的物质的量浓度为0.05 mol/L |
考点:物质的量浓度
专题:物质的量浓度和溶解度专题
分析:A、322 g Na2SO4?10H2O物质的量为1mol,溶于1 L水中溶液体积大于1L;
B、依据稀释溶液后溶质物质的量不变计算分析;
C、18.4 mol/L的H2SO4溶液密度大于1,和水等体积混合,溶质浓度大于平均值;
D、气体体积不是标准状况,溶质不一定是0.015mol.
B、依据稀释溶液后溶质物质的量不变计算分析;
C、18.4 mol/L的H2SO4溶液密度大于1,和水等体积混合,溶质浓度大于平均值;
D、气体体积不是标准状况,溶质不一定是0.015mol.
解答:
解:A、322 g Na2SO4?10H2O物质的量为1mol,溶于1 L水中溶液体积大于1L,所得溶液的物质的量浓度小于1 mol/L,故A错误;
B、依据稀释溶液后溶质物质的量不变计算,将1 L 2 mol/L H2SO4溶液加水稀释到2 L,所得溶液的物质的量浓度为1 mol/L,故B正确;
C、18.4 mol/L的H2SO4溶液密度大于1,和水等体积混合,溶质浓度大于平均值,将1 L 18.4 mol/L的H2SO4溶液加入到1 L水中,所得溶液的物质的量浓度大于9.2 mol/L,故C错误;
D、气体体积不是标准状况,溶质不一定是0.015mol,故D错误;
故选B.
B、依据稀释溶液后溶质物质的量不变计算,将1 L 2 mol/L H2SO4溶液加水稀释到2 L,所得溶液的物质的量浓度为1 mol/L,故B正确;
C、18.4 mol/L的H2SO4溶液密度大于1,和水等体积混合,溶质浓度大于平均值,将1 L 18.4 mol/L的H2SO4溶液加入到1 L水中,所得溶液的物质的量浓度大于9.2 mol/L,故C错误;
D、气体体积不是标准状况,溶质不一定是0.015mol,故D错误;
故选B.
点评:本题考查物质的量、物质的量浓度计算,比较基础,侧重对基础知识的巩固,注意对公式的理解与灵活应用,注意溶液密度对混合溶液的影响,题目较简单.

练习册系列答案
相关题目
下列物质中,属于芳香烃且属于苯的同系物的是( )
A、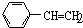 |
B、 |
C、 |
| D、CH≡C-C≡CH |
提纯含有少量NaCl杂质的KNO3固体,涉及的操作可能有:①将需要提纯的固体溶解在80℃以上的热水中达到饱和;②加热蒸发;③冷却;④结晶;⑤过滤.合理的操作步骤是( )
| A、①②③④ | B、①③⑤② |
| C、②③④⑤ | D、①③④⑤ |
下列叙述中正确的是( )
| A、离子化合物中可能含有非极性键 |
| B、以极性键结合的分子一定是极性分子 |
| C、非极性分子只能是单质分子 |
| D、非极性分子中一定含有非极性键 |
可以用分液漏斗分离的一组液体是( )
| A、苯和汽油 | B、苯和溴苯 |
| C、水和甲苯 | D、溴和四氯化碳 |
能加快石灰石和盐酸反应速率的是( )
| A、加大盐酸用量 |
| B、增大盐酸浓度 |
| C、使用块状石灰石 |
| D、增大体系压强 |
下列叙述正确的是( )
| A、汽油、柴油和植物油都是碳氢化合物 |
| B、用于包装食品的塑料通常是聚氯乙烯 |
| C、聚乙烯可做不粘锅的内衬材料 |
| D、塑料在自然环境下不易分解,可造成白色污染 |
下列说法正确的是 ( )
| A、减小反应物的浓度、降低反应温度都能使化学反应速率减小 |
| B、可逆反应达到化学平衡状态(即最大限度)时,反应物和生成物的浓度一定相等 |
| C、可逆反应达到化学平衡状态时,反应停止,正、逆反应速率都为零 |
| D、在500℃和催化剂作用下,固定容积的密闭容器内的SO2和O2能全部变为SO3? |
关于烃和甲烷的叙述正确的是( )
| A、烃的组成均符合通式CnH2n+2 |
| B、甲烷在同系物中含碳量最高,因而是清洁能源 |
| C、烃类分子中的碳原子与其它原子的结合方式是形成四对共用电子对 |
| D、甲烷不能发生氧化反应 |