题目内容
2. 随着对合成氨研究的发展,希腊科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如图).钯电极A是电解池的阴极(填“阳”或“阴”),该极上的电极反应式是N2+6e-+6H+═2NH3.
随着对合成氨研究的发展,希腊科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如图).钯电极A是电解池的阴极(填“阳”或“阴”),该极上的电极反应式是N2+6e-+6H+═2NH3.
分析 根据合成反应的条件和水的状态角度来考虑,根据电解池的工作原理:电解池的阴极发生得电子的还原反应,氢离子移向阴极,从B电极移向A电极.
解答 解:用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如图),氢离子移向阴极,从B电极移向A电极,说明钯电极A是电解池的阴极,氨气发生氧化反应:N2+6e-+6H+═2NH3,
故答案为:阴; N2+6e-+6H+═2NH3.
点评 本题考查了电解原理的分析应用,主要是电极反应书写、离子移向等知识的判断,掌握基础是解题关键,题目难度不大.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
13.用惰性电极电解下列溶液,电解一段时间后,电解液的pH增大了的是( )
| A. | H2SO4 | B. | Na2SO4 | C. | AgNO3 | D. | KOH |
17.室温时将浓度和体积分别为 c1、V1的 NaOH 溶液和 c2、V2的 CH3COOH 溶液相混合,下列关于该混合溶液的叙述错误的是( )
| A. | 若 pH>7,则一定是 c1V1═c2V2 | |
| B. | 在任何情况下都是 c(Na+)+c(H+)═c(CH3COO-)+c(OH-) | |
| C. | 当 pH=7 时,若 V1=V2,则一定是 c1<c2 | |
| D. | 若 V1=V2、c1=c2,则 c(CH3COO-)+c(CH3COOH)═c(Na+) |
7.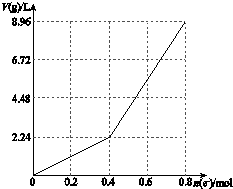 以石墨电极电解200mL CuSO4溶液,电解过程中电子转移物质的量n(e-)与产生气体体积V(g)(标准状况)的关系如图所示.下列说法中,正确的是( )
以石墨电极电解200mL CuSO4溶液,电解过程中电子转移物质的量n(e-)与产生气体体积V(g)(标准状况)的关系如图所示.下列说法中,正确的是( )
 以石墨电极电解200mL CuSO4溶液,电解过程中电子转移物质的量n(e-)与产生气体体积V(g)(标准状况)的关系如图所示.下列说法中,正确的是( )
以石墨电极电解200mL CuSO4溶液,电解过程中电子转移物质的量n(e-)与产生气体体积V(g)(标准状况)的关系如图所示.下列说法中,正确的是( )| A. | 电解前CuSO4溶液的物质的量浓度为2 mol/L | |
| B. | 电解后所得溶液中c(H+)=1 mol/L | |
| C. | 当n(e-)=0.6 mol时,V(H2):V(O2)=2:3 | |
| D. | 向电解后的溶液中加入16 g CuO,则溶液可恢复为电解前的浓度 |
14.某溶液里加入过量氨水或过量的NaOH溶液均有沉淀产生,若加入铁粉或铜粉溶液质量都增加,则溶液中可能含下列的( )
| A. | Al3+ | B. | Fe2+ | C. | Fe3+ | D. | Mg2+ |
11.如图是酷似奥林匹克旗中五环的一种有机物,被称之为奥林匹克烃,下列说法正确的是( )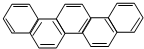

| A. | 该有机物属于苯的同系物 | |
| B. | 1mol该有机物最多可以和15molH2反应 | |
| C. | 该有机物的一氯代物有一种 | |
| D. | 该有机物完全燃烧生成H2O 的物质的量小于CO2的物质的量 |
12.将Zn和Cu用导线连接置于同一稀硫酸溶液中,下列叙述正确的是( )
| A. | H+被氧化 | B. | SO42-向正极移动 | C. | Cu片逐渐溶解 | D. | 溶液酸性减弱 |