题目内容
10.一种新型熔融盐燃料电池具有高发电效率.现用Li2CO3和Na2CO3的熔融盐混合物作电解质,一极通CO气体,另一极通O2和CO2混合气体,其总反应为:2CO+O2═2CO2.则下列说法中正确的是( )| A. | CO32-向正极移动 | |
| B. | 负极发生的电极反应是:O2+2CO2+4e-═2CO32- | |
| C. | 负极发生的电极反应是:CO+CO32--2e-═2CO2 | |
| D. | 正极发生氧化反应 |
分析 该燃料电池中,通入CO的一极为原电池的负极,发生氧化反应,电极反应式为2CO-4e-+2CO32-═4CO2,通入氧气和CO2的混合气体一极为原电池的正极,发生还原反应,电极反应式为O2+4e-+2CO2═2CO32-,阴离子移向负极,据此分析判断.
解答 解:A、阴离子移向负极,所以CO32-向负极移动,故A错误;
B、通入CO的一极为原电池的负极,发生氧化反应,电极反应式为CO-2e-+CO32-═2CO2,故B错误;
C、通入CO的一极为原电池的负极,发生氧化反应,电极反应式为CO+CO32--2e-═2CO2,故C正确;
D、通入氧气和CO2的混合气体一极为原电池的正极,发生还原反应,故D错误;
故选:C.
点评 本题考查原电池原理,根据燃料电池的工作原理规律来分析解答即可,注意电极反应式的正确书写,为易错点.

练习册系列答案
相关题目
20.下列化学方程式中,书写正确的是( )
| A. | Al+O2$\frac{\underline{\;点燃\;}}{\;}$AlO2 | B. | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 | ||
| C. | 2H2O═2H2+O2 | D. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2↑ |
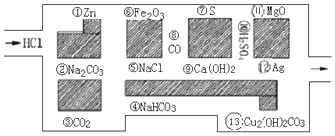
1.观察下列几个装置示意图,有关叙述正确的是( )


| A. | 装置②的待镀铁制品应与电源正极相连 | |
| B. | 装置①中阴极上析出红色固体 | |
| C. | 装置③闭合开关后,外电路电子由a极流向b极 | |
| D. | 装置④的X电极是外接电源的正极 |
5.R、T、X、Y、Z是短周期元素,它们的原子序数依次增大.R、X原子的最外层电子数相等,R的阴离子与氦原子的电子层结构相同;T原子的最外层电子数与电子层数之比为3,XYT2能促进水的电离;Z的原子序数等于T原子最外层电子数与X原子的电子数之和.下列推断不正确的是( )
| A. | Z位于周期表第三周期第ⅦA族 | |
| B. | 简单离子半径由大到小排序:Z、T、X、Y | |
| C. | X、Y、Z的最高价氧化物对应的水化物能相互反应 | |
| D. | R2T2和X2T2中所含化学键类型完全相同 |

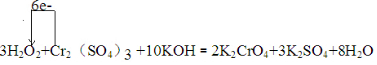 .
.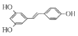 )具有预防心血管疾病的作用,其一种合成路线如图:
)具有预防心血管疾病的作用,其一种合成路线如图: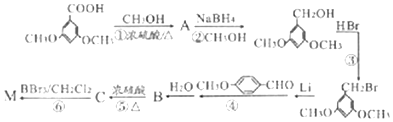
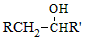
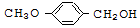 $\stackrel{BBr_{3}/CH_{2}Cl_{2}}{→}$
$\stackrel{BBr_{3}/CH_{2}Cl_{2}}{→}$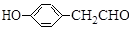 回答下列问题:
回答下列问题: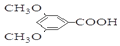 核磁共振氢谱中不同化学环境的氢原子个数比为6:1:2:1.
核磁共振氢谱中不同化学环境的氢原子个数比为6:1:2:1. .
. .
.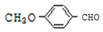 有多种同分异构体,其中能发生银镜反应且苯环上一氯取代物只有两种的同分异构体有3种.
有多种同分异构体,其中能发生银镜反应且苯环上一氯取代物只有两种的同分异构体有3种.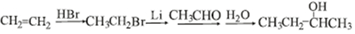 .
.