题目内容
20.硫酸镁、硫酸铝两种物质组成的混合溶液 100mL 中,SO42- 的物质的量浓度为0.10mol/L,加入0.30mol/L NaOH 溶液到生成的白色沉淀恰好不再溶解为止,消耗NaOH溶液的体积为100mL,过滤,所得滤液中AlO2- 的物质的量浓度为多少?分析 硫酸镁、硫酸铝溶液中加入氢氧化钠到生成的白色沉淀恰好不再溶解为止,此时得到物质为氢氧化镁、硫酸钠和偏铝酸钠,依据反应过程中硫酸根离子守恒和钠离子守恒计算解答.
解答 解:据题意硫酸镁、硫酸铝两种物质组成的混合溶液 100mL 中,SO42- 的物质的量浓度为0.10mol/L,则溶液中含有硫酸根离子的物质的量为0.10 mol/L×0.1 L=0.01 mol,反应消耗的氢氧化钠的物质的量为:0.30mol/L×0.1L=0.03mol,反应后生成Mg(OH)2 沉淀、Na2SO4 溶液、NaAlO2溶液,依据硫酸根离子守恒可知:生成硫酸钠物质的量为0.1mol,据Na+守恒有n(NaAlO2)=0.30 mol/L×0.1 L-0.01 mol×2=0.01 mol,
c(AlO2-)=$\frac{n(NaAlO2)}{V}$=$\frac{0.01mol}{0.2L}$=0.05 mol/L.
故答案:0.05 mol/L.
点评 本题考查了有关物质的量浓度计算,明确发生的反应,准确判断生成产物,依据原子个数守恒即可解答,题目难度不大.

练习册系列答案
相关题目
10.下列叙述中正确的是( )
| A. | 氯化钠中混有少量单质碘杂质,可用升华的方法提纯 | |
| B. | 能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2 | |
| C. | SO2可使酸性高锰酸钾溶液褪色,体现了SO2的漂白性 | |
| D. | 浓硫酸具有吸水性,可以用作干燥剂,例如可用于NH3的干燥 |
11.下列结论中错误的是( )
①微粒半径:K+>Al3+>Cl-
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:F->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO
⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K.
①微粒半径:K+>Al3+>Cl-
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:F->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO
⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K.
| A. | ① | B. | ①③ | C. | ②④⑤⑥⑦ | D. | ①③⑤ |
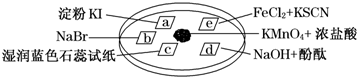
15.如图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸.向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面.
已知:2KMnO4+16HCl(浓)═2KCl+5Cl2↑+2MnCl2+8H2O
对实验现象的“解释或结论”正确的是( )
已知:2KMnO4+16HCl(浓)═2KCl+5Cl2↑+2MnCl2+8H2O

对实验现象的“解释或结论”正确的是( )
| 选项 | 实验现象 | 解释或结论 |
| A | a处变蓝 | 氧化性:Cl2>I2 |
| B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
| C | d处立即褪色 | 氯气与水生成了漂白性物质 |
| D | e处变血红色 | 还原性:Fe2+>Cl- |
| A. | A | B. | B | C. | C | D. | D |
5.下列化学用品的安全警示性标注正确的是( )
| A. | 酒精──剧毒品 | B. | 浓硫酸──剧毒品 | C. | 汽油──易燃品 | D. | 浓盐酸──易燃品 |
12.下列说法不正确的是( )
| A. | 分解反应肯定是吸热反应 | |
| B. | 物质燃烧和中和反应均放出热量 | |
| C. | 化学反应除了生成新物质外,还伴随着能量的变化 | |
| D. | 化学反应是吸热还是放热决定于生成物和反应物具有的总能量大小 |
9.下列各组物质的主要成分皆为同一种酸所对应的盐的是( )
| A. | 大理石 钡餐 石膏 | B. | 小苏打 苏打 水玻璃 | ||
| C. | 芒硝 胆矾 明矾 | D. | 黄铜矿 硫铁矿 磁铁矿 |
7.室温下,0.1mol•L-1NaHCO3溶液的pH=8.31,有关该溶液的判断正确的是( )
| A. | c(Na+)>c(OH-)>c(HCO3-)>c(CO32-)>c(H+) | |
| B. | c(H+)+c(Na+)=c(OH-)+c(HCO3-)+c(CO32-) | |
| C. | 加入适量NaOH溶液后:c(Na+)=c(H2CO3)+c(HCO3-)+c(CO32-) | |
| D. | Ka1(H2CO3)•Ka2(H2CO3)<Kw |