题目内容
(2011?佛山一模)高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂.
(1)请完成FeO42-与水反应的方程式:
4FeO42-+10H2O?4Fe(OH)3+8OH-+
(2)将适量K2FeO4配制成c(FeO42-)=1.0mmol?L-1的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(FeO42-)的变化,结果见图Ⅰ.第(1)题中的反应为FeO42-变化的主反应,则温度对该反应的反应速率和平衡移动的影响是
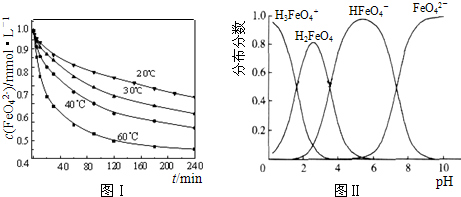
(3)FeO42-在水溶液中的存在形态如图Ⅱ所示.下列说法正确的是
A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.向pH=2的这种溶液中加KOH溶液至pH=10,HFeO4-的分布分数先增大后减小
C.向pH=8的这种溶液中加KOH溶液,发生反应的离子方程式为:H2FeO4+OH-=HFeO4-+H2O
(4)H2FeO4?H++HFeO4-的电离平衡常数表达式为K=
.
(1)请完成FeO42-与水反应的方程式:
4FeO42-+10H2O?4Fe(OH)3+8OH-+
3O2
3O2
.K2FeO4在处理水的过程中所起的作用是杀菌消毒
杀菌消毒
和吸附悬浮物
吸附悬浮物
.(2)将适量K2FeO4配制成c(FeO42-)=1.0mmol?L-1的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(FeO42-)的变化,结果见图Ⅰ.第(1)题中的反应为FeO42-变化的主反应,则温度对该反应的反应速率和平衡移动的影响是
温度升高,反应速率加快,平衡向正反应方向移动
温度升高,反应速率加快,平衡向正反应方向移动
;发生反应的△H>
>
0(填“>”、“<”或“=”).
(3)FeO42-在水溶液中的存在形态如图Ⅱ所示.下列说法正确的是
B
B
(填字母).A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.向pH=2的这种溶液中加KOH溶液至pH=10,HFeO4-的分布分数先增大后减小
C.向pH=8的这种溶液中加KOH溶液,发生反应的离子方程式为:H2FeO4+OH-=HFeO4-+H2O
(4)H2FeO4?H++HFeO4-的电离平衡常数表达式为K=
| c(H+).c(FeO42-) |
| c(HFeO4-) |
| c(H+).c(FeO42-) |
| c(HFeO4-) |
分析:(1)根据元素守恒和化合价的变化分析;高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂,起到杀菌消毒作用,形成胶体具有吸附悬浮杂质的作用;
(2)温度越高,相同时间内FeO42-浓度变化越快,高铁酸钾溶液平衡时FeO42-浓度越小;温度越高FeO42-浓度越小,正向反应是吸热反应;
(3)根据图象的内容来分析图象所描述的意义;
(4)平衡常数等于生成物浓度幂之积与反应物浓度幂之积的比;
(2)温度越高,相同时间内FeO42-浓度变化越快,高铁酸钾溶液平衡时FeO42-浓度越小;温度越高FeO42-浓度越小,正向反应是吸热反应;
(3)根据图象的内容来分析图象所描述的意义;
(4)平衡常数等于生成物浓度幂之积与反应物浓度幂之积的比;
解答:解:(1)根据元素守恒可知未知产物应含氧元素,反应中Fe元素化合价降低,则氧元素化合价升高,所以产物为氧气,根据原子守恒可知为3O2;高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂,起到杀菌消毒作用,形成胶体具有吸附悬浮杂质的作用;
故答案为:3O2;杀菌消毒、吸附悬浮物;
(2)由图1数据可知,温度越高,相同时间内FeO42-浓度变化越快,高铁酸钾溶液平衡时FeO42-浓度越小,温度越高FeO42-浓度越小,正向反应是吸热反应;
故答案为:温度升高,反应速率加快,平衡向正反应方向移动;>;
(3)A、不同PH值时,溶液中铁元素的存在形态及种数不相同,比如在PH值等于6时,就只有两种形态,故A错误;
B.根据图片知,改变溶液的pH,当溶液由pH=10降至pH=4的过程中,HFeO4-的分布分数先增大后减小,故正确;
C.向pH=8的这种溶液中加KOH溶液,发生反应的离子方程式为:HFeO4-+OH-=FeO42-+H2O,故错误;
故答案为:B;
(4)HFeO4-?H++FeO42-的电离平衡常数表达式为K=
,
故答案为:
.
故答案为:3O2;杀菌消毒、吸附悬浮物;
(2)由图1数据可知,温度越高,相同时间内FeO42-浓度变化越快,高铁酸钾溶液平衡时FeO42-浓度越小,温度越高FeO42-浓度越小,正向反应是吸热反应;
故答案为:温度升高,反应速率加快,平衡向正反应方向移动;>;
(3)A、不同PH值时,溶液中铁元素的存在形态及种数不相同,比如在PH值等于6时,就只有两种形态,故A错误;
B.根据图片知,改变溶液的pH,当溶液由pH=10降至pH=4的过程中,HFeO4-的分布分数先增大后减小,故正确;
C.向pH=8的这种溶液中加KOH溶液,发生反应的离子方程式为:HFeO4-+OH-=FeO42-+H2O,故错误;
故答案为:B;
(4)HFeO4-?H++FeO42-的电离平衡常数表达式为K=
| c(H+).c(FeO42-) |
| c(HFeO4-) |
故答案为:
| c(H+).c(FeO42-) |
| c(HFeO4-) |
点评:本题考查了缺项方程式的配平、电离平衡、温度对平衡的影响等知识点,难度中等,注意对图象的分析是解题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目



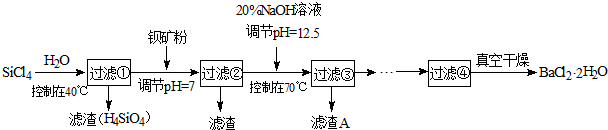
 (2011?佛山一模)纯碱、烧碱等是重要的化工原料.
(2011?佛山一模)纯碱、烧碱等是重要的化工原料.