题目内容
设NA为阿伏伽德罗常数的值。下列说正确的是
A.高温下,0.2molFe与足量水蒸气反应,生成的H2分子数目为0.3NA
B.标准状况下,22.4L盐酸含有NA个HCl分子
C.氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA
D.5NH4NO3 === 2HNO3+4N2↑+9H2O反应中,生成28g N2时,转移的电子数目为3.75NA
D
【解析】
试题分析:A.0.2mol铁与水蒸气完全反应生成四氧化三铁,失去电子的物质的量为:(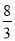 -0)×0.2mol=
-0)×0.2mol=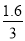 mol,根据电子守恒,生成氢气的物质的量为:
mol,根据电子守恒,生成氢气的物质的量为: mol÷2=
mol÷2= mol,生成的H2分子数目为
mol,生成的H2分子数目为 NA,故A错误;B.在溶液中氯化氢完全电离,不存在氯化氢分子,故B错误;C.氢氧燃料电池中,正极氧气得到电子,标况下22.4L氧气的物质的量为1mol,1mol氧气完全反应得到4mol电子,电路中通过的电子数目为4NA,故C错误;D.该氧化还原反应中,生成4mol氮气转移了15mol电子,28g氮气的物质的量为1mol,生成1mol氮气转移的电子的物质的量为:15mol÷4=3.75mol,转移的电子数目为3.75NA,故D正确;故选D。
NA,故A错误;B.在溶液中氯化氢完全电离,不存在氯化氢分子,故B错误;C.氢氧燃料电池中,正极氧气得到电子,标况下22.4L氧气的物质的量为1mol,1mol氧气完全反应得到4mol电子,电路中通过的电子数目为4NA,故C错误;D.该氧化还原反应中,生成4mol氮气转移了15mol电子,28g氮气的物质的量为1mol,生成1mol氮气转移的电子的物质的量为:15mol÷4=3.75mol,转移的电子数目为3.75NA,故D正确;故选D。
考点:考查阿伏加德罗常数的有关计算和判断

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案
相关题目
 )。
)。


