题目内容
有六种离子:①S2- ②Fe2+ ③S ④I- ⑤H+ ⑥Fe3+,请回答(填编号):
(1)只有氧化性的是 ;
(2)只有还原性的是 ;
(3)既有氧化性,又有还原性的是 ;
(4)请从(1)、(2)中各选取一种离子,它们之间能发生氧化还原反应,并写出该反应的离子方程式 .
(1)只有氧化性的是
(2)只有还原性的是
(3)既有氧化性,又有还原性的是
(4)请从(1)、(2)中各选取一种离子,它们之间能发生氧化还原反应,并写出该反应的离子方程式
考点:氧化还原反应
专题:氧化还原反应专题
分析:由元素的化合价可知,处于最高价的元素的微粒具有氧化性,处于最低价的元素的微粒具有还原性,而处于中间价态的微粒既有氧化性又有还原性,以此来解答.
解答:
解:处于最高价的元素的微粒具有氧化性,处于最低价的元素的微粒具有还原性,而处于中间价态的微粒既有氧化性又有还原性,则
(1)H+、Fe3+元素化合价为最高价态,只有氧化性,故答案为:⑤⑥;
(2)S2-、I-元素化合价处于最低价态,只具有还原性,故答案为:①④;
(3)Fe2+、S元素化合价处于中间价态,既有氧化性又有还原性,故答案为:②③;
(4)Fe3+具有氧化性,可氧化S2-或I-,如发生2Fe3++2I-=2Fe2++I2或2Fe3++S2-=2Fe2++S,故答案为:2Fe3++2I-=2Fe2++I2或2Fe3++S2-=2Fe2++S.
(1)H+、Fe3+元素化合价为最高价态,只有氧化性,故答案为:⑤⑥;
(2)S2-、I-元素化合价处于最低价态,只具有还原性,故答案为:①④;
(3)Fe2+、S元素化合价处于中间价态,既有氧化性又有还原性,故答案为:②③;
(4)Fe3+具有氧化性,可氧化S2-或I-,如发生2Fe3++2I-=2Fe2++I2或2Fe3++S2-=2Fe2++S,故答案为:2Fe3++2I-=2Fe2++I2或2Fe3++S2-=2Fe2++S.
点评:本题考查氧化还原反应,为高频考点,侧重学生的分析能力的考查,主要从元素化合价的角度认识物质的性质,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
有机化学中取代反应范畴很广,下列3个反应中,属于取代反应范畴的是(填写相应的字母) ( )
A、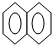 +HNO3 +HNO3
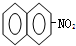 +H2O +H2O | |||
B、
| |||
C、2CH3CH2OH
|
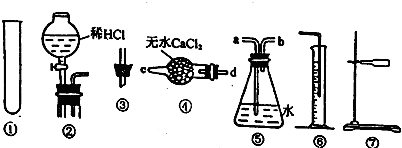
 某校化学兴趣小组对一款锌铁合金中铁的含量进行测定,该小组提出用测定产生氢气的体积的方法来进行实验.实验过程中需要读取氢气体积.
某校化学兴趣小组对一款锌铁合金中铁的含量进行测定,该小组提出用测定产生氢气的体积的方法来进行实验.实验过程中需要读取氢气体积.