题目内容
12.药物阿司匹林可由水杨酸制得,它们的结构如图所示.下列有关说法正确的是( )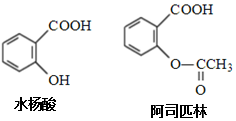
| A. | 阿司匹林分子中存在碳碳双键和碳氧双键 | |
| B. | 阿司匹林的分子式为C9H10O4,能与NaHCO3反应 | |
| C. | 水杨酸可以发生取代反应和加成反应 | |
| D. | 水杨酸的同分异构体中,含有羧基和羟基的只有2种 |
分析 A.阿司匹林分子不含碳碳双键;
B.阿司匹林的分子式为C9H8O4;
C.水杨酸含有苯环、羧基、羟基结合苯、酚、酸的性质判断;
D.羧基和羟基可位于苯环的邻、间、对位置.
解答 解:A.阿司匹林分子含有苯环、C=O,不含碳碳双键,故A错误;
B.由结构简式可知阿司匹林的分子式为C9H8O4,故B错误;
C.水杨酸含有苯环,可发生加成反应,含有羧基、羟基,可发生取代反应,故C正确;
D.羧基和羟基可位于苯环的邻、间、对位置,则水杨酸的同分异构体中,含有羧基和羟基的有3种,故D错误.
故选C.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重于学生的分析能力的考查,注意把握有机物的结构和官能团的性质,为解答该类题目的关键,难度不大.

练习册系列答案
相关题目
2.化学与科学、技术、社会、环境密切关.下列叙述不正确的是( )
| A. | 大气中PM2.5比表面积大,吸附力强,能吸附许多有毒、有害物质 | |
| B. | Na2S具有还原性,作废水中Cu2+、Hg2+沉淀剂 | |
| C. | 石墨烯一种由单层碳原子构成的新纳米材料,具有导电性 | |
| D. | 刚玉、红宝石主要或分是氧化铝,陶瓷、分子筛主要成分是硅酸盐 |
3.某温度下反应N2O4(g)?2NO2(g)(正反应为吸热反应),在密闭容器中达到平衡,下列说法正确的是( )
①加压时(体积变小),将使正反应速率增大
②保持体积不变,加入少许NO2,将使正反应减小;
③保持体积不变,加入少许N2O4,再达到平衡时颜色变深;
④保持体积不变,升高温度,再达平衡时颜色变深
⑤升高温度,正反应速率减小,平衡逆向移动.
①加压时(体积变小),将使正反应速率增大
②保持体积不变,加入少许NO2,将使正反应减小;
③保持体积不变,加入少许N2O4,再达到平衡时颜色变深;
④保持体积不变,升高温度,再达平衡时颜色变深
⑤升高温度,正反应速率减小,平衡逆向移动.
| A. | ①④⑤ | B. | ③④⑤ | C. | ①③④ | D. | ①②③④⑤ |
20.在原电池和电解池的电极上所发生反应的类型相同的是( )
| A. | 原电池的正极和电解池阳极 | B. | 电解池阳极和电解池阴极 | ||
| C. | 原电池负极和电解池阳极 | D. | 原电池的正极和原电池负极 |
7.短周期的三种元素A、B、C在周期表中的位置关系如图,下列有关A、B、C三种元素的叙述中正确的是
( )
( )
| A | ||
| B | ||
| C |
| A. | A是一种活泼金属元素 | |
| B. | C的最高价氧化物的水化物是强酸 | |
| C. | B的氢氧化物是强碱 | |
| D. | C的最高价氧化物对应的水化物能与NaOH溶液反应 |
17.下列相关实验示意图不能达到实验目的是( )
| A. | 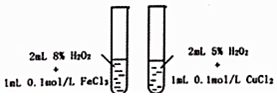 探究不同催化剂对H2O分解速率影响 | |
| B. | 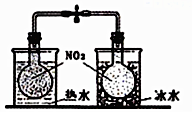 探究温度对2NO2?N2O2平衡影响 | |
| C. |  验证Cr2O72-+H2O?2CrO42-+H+平衡状态变化 | |
| D. |  验证钠和水反应的热效应 |
4.下列说法中正确的是( )
| A. | 烷烃中除甲烷外,很多烷烃都能被酸性KMnO4溶液氧化 | |
| B. | 烯烃、炔烃、苯都能发生化学反应使溴的四氯化碳溶液褪色 | |
| C. | 乙烯、乙炔、乙烷的分子中所有原子都在同一平面上 | |
| D. | 乙烷和丙烯的物质的量共1 mol,完全燃烧生成3 molH2O |
1.一定温度下,将 2mol SO2 和 1mol O2充入一定容密闭容器中,在催化剂存在下进行下列反应:2SO2(g)+O2(g)?2SO3(g);当达到平衡状态时,下列说法中正确的是( )
| A. | 生成 SO3 为2 mol | |
| B. | 反应完全停止 | |
| C. | SO2 和 SO3物质的量之和为 2mol | |
| D. | SO2 的物质的量和SO3物质的量相等 |
17.某有机化合物的结构简式如图所示,下列说法正确的是( )
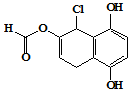

| A. | 不能发生银镜发应,能发生水解反应 | |
| B. | 1mol 该物质最多可与含2mol溴单质的浓溴水反应 | |
| C. | 1mol 该物质最多可与4molNaOH反应 | |
| D. | 与Na、NaHCO3、Na2CO3均能发生反应 |