题目内容
下列离子方程式不正确的是( )
| A、FeCl2溶液和Cl2反应:2Fe2++Cl2=2Fe3++2Cl- |
| B、钠与水反应:Na+H2O=Na++OH-+H2↑ |
| C、Na2CO3溶液与足量盐酸反应:CO32-+2H+==CO2↑+H2O |
| D、NaHCO3溶液与NaOH溶液:HCO3-+OH-=CO32-+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.氯气具有强氧化性,通入FeCl2溶液反应生成氯化铁;
B.没有配平,左右氢原子不守恒;
C.Na2CO3溶液与足量盐酸反应生成氯化钠和水、二氧化碳;
D.NaHCO3与NaOH溶液反应实质为碳酸氢根离子与氢氧根离子反应生成碳酸根离子和水;
B.没有配平,左右氢原子不守恒;
C.Na2CO3溶液与足量盐酸反应生成氯化钠和水、二氧化碳;
D.NaHCO3与NaOH溶液反应实质为碳酸氢根离子与氢氧根离子反应生成碳酸根离子和水;
解答:
解:A.氯气具有强氧化性,通入FeCl2溶液反应生成氯化铁,离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,故A正确;
B.少量金属钠放到冷水中的离子反应为2Na+2H2O=2Na++2OH-+H2↑,故B错误;
C.Na2CO3为可溶性的碳酸盐完全电离,与足量盐酸反应CO32-+2H+==CO2↑+H2O,故C正确;
D.NaHCO3溶液与NaOH溶液反应生成可溶性的碳酸钠和水,反应的实质为HCO3-与OH-反应生成CO32-和H2O,该反应的离子方程式为:OH-+HCO3-=CO32-+H2O,故D正确;
故选B.
B.少量金属钠放到冷水中的离子反应为2Na+2H2O=2Na++2OH-+H2↑,故B错误;
C.Na2CO3为可溶性的碳酸盐完全电离,与足量盐酸反应CO32-+2H+==CO2↑+H2O,故C正确;
D.NaHCO3溶液与NaOH溶液反应生成可溶性的碳酸钠和水,反应的实质为HCO3-与OH-反应生成CO32-和H2O,该反应的离子方程式为:OH-+HCO3-=CO32-+H2O,故D正确;
故选B.
点评:本题考查离子反应方程式的书写,明确发生的化学反应是解答本题的关键,注意选项D碳酸氢钠为多元弱酸的酸式盐碳酸氢根离子不能拆为解答的难点和易错点,注意离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
如图所示,A、B、C、D、E是元素周期表中的5种主族元素,下列说法不正确的是( )
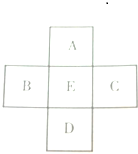

| A、A、E原子序数之差可能为2 |
| B、D、E原子序数之差可能为18或32 |
| C、B、C原子序数之差一定是2 |
| D、B、D原子序数之差不可能是7 |
下列方程式错误的是( )
| A、0.1mol?L-1CH3COOH溶液的pH为3:CH3COOH?H++CH3COO- | ||||
| B、A1Cl3溶液中加入过量稀氨水:A13++3NH3?H2O═A1(OH)3↓+3 NH4+ | ||||
C、C12与过量的铁反应:3C12+2Fe
| ||||
| D、NaHCO3溶液中加入稀盐酸:CO32一+2H+═CO2↑+H2O |
某溶液能与Al片作用出氢气,则该溶液可能大量共存的离子组合是.( )
| A、Na+、NO3-、K+、Fe2+ |
| B、Fe2+、Na+、Cl-、K+ |
| C、K+、I-、NO3-、H+ |
| D、NH4+、NO3-、Na+、SO3- |
分类是重要的科学研究方法,下列物质分类不正确的是( )
| A、电解质:明矾、一水合氨、硫酸钡 |
| B、酸性氧化物:CO2、SO2、NO2、SiO2 |
| C、混合物:铝热剂、矿泉水、水玻璃、漂白粉 |
| D、同素异形体:C60、C70、金刚石 |
下列离子方程式正确的是( )
| A、钠投入水中:Na+H2O=Na++OH-+H2↑ |
| B、铜与稀硫酸反应:Cu+2H+=Cu2++H2↑ |
| C、石灰石溶于盐酸中:CaCO3+2H+=Ca2++CO2↑+H2O |
| D、氢氧化钡溶液与稀硫酸混合:Ba2++2H++2OH-+SO42-=BaSO4↓+2H2O |
在恒容密闭容器中发生反应2NO2?2NO+O2,不能说明反应达到平衡状态的是( )
| A、单位时间内生成n molO2的同时生成2n molNO2 |
| B、单位时间内生成n molO2的同时生成2n molNO |
| C、混合气体的颜色不再改变 |
| D、氧气的含量不再改变 |
 如图是某有机物分子的比例模型,黑色的是碳原子,白色的是氢原子,灰色的是氧原子.则该物质不具有的性质是( )
如图是某有机物分子的比例模型,黑色的是碳原子,白色的是氢原子,灰色的是氧原子.则该物质不具有的性质是( )| A、使紫色石蕊变红 |
| B、与钠反应 |
| C、发生酯化反应 |
| D、发生氧化反应 |