题目内容
下列说法正确的是( )

| A、1mol白磷晶体中含有的P-P键的个数为4NA |
| B、12g金刚石中含有的C-C键的个数为1.5NA |
| C、12g石墨烯(单层石墨)中含有六元环的个数为0.5NA |
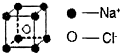
| D、1mol氯化钠(晶胞如图)中含有Na+数目为8NA |
考点:不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:A、根据P4是正四面体结构进行分析;
B、根据1mol金刚石含有2molC-C键进行判断;
C、依据n=
计算物质的量,结合石墨烯中平均每个六元环含碳原子2个;
D、根据均摊法计算.
B、根据1mol金刚石含有2molC-C键进行判断;
C、依据n=
| m |
| M |
D、根据均摊法计算.
解答:
解:A、P4是正四面体结构,1mol P4含有P-P键含有6mol共价键,含有p-P键的个数为6NA,故A错误;
B、金刚石中的碳都是与相邻的4个碳组成的四个共价键,但是每个共价键是两个C原子共用的,所以1mol碳原子就有2mol的C-C键;12g金刚石中含有1molC原子,含有C-C键的个数为2NA,故B错误;
C、依据n=
计算物质的量=
=1mol,石墨烯中平均每个六元环含碳原子2个,则1mol碳原子含有六元环的个数为0.5NA,故C正确;
D、晶胞中Na+数为8×
=1,1mol氯化钠(晶胞如图)中含有Na+数目为NA,故D错误.
B、金刚石中的碳都是与相邻的4个碳组成的四个共价键,但是每个共价键是两个C原子共用的,所以1mol碳原子就有2mol的C-C键;12g金刚石中含有1molC原子,含有C-C键的个数为2NA,故B错误;
C、依据n=
| m |
| M |
| 12g |
| 12g/mol |
D、晶胞中Na+数为8×
| 1 |
| 8 |
点评:本题考查了阿伏伽德罗常数,注意根据原子晶体的结构分析晶体中含有的化学键数目,本题难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
化学与生活密切相连,下列说法正确的是( )
| A、送外卖人员用聚氯乙烯生产的塑料袋盛热汤 |
| B、用新制氢氧化铜悬浊液检验病人是否患糖尿病 |
| C、“地沟油”、“塑化剂”(邻苯二甲酸酯类物质)均属于高分子化合物,都对健康有害 |
| D、磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 |
在相同温度下,已知2H2(g)+O2(g)=2H2O(g)△H1; 2H2(g)+O2(g)=2H2O(l)△H2;H2(g)+
O2(g)=H2O(l)△H3,则△H1、△H2、△H3大小关系为( )
| 1 |
| 2 |
| A、△H1=△H2=△H3 |
| B、2△H3=△H2>△H1 |
| C、△H3>△H2>△H1 |
| D、2|△H3|=|△H2|>|△H1| |
下列指定反应的离子方程式,正确的是( )
| A、氢氧化亚铁溶于稀硝酸中:Fe (OH)2+2H+═Fe2++2H2O |
| B、碳酸钙溶于稀醋酸溶液:CaCO3+2H+═Ca2++CO2↑+H2O |
| C、向NH4Al (SO4)2溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀:2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O |
| D、向苯酚钠溶液中通入少量的CO2:C6H5O-+CO2+H2O→C6H5OH+HCO3- |
下列说法正确的是( )
| A、纤维素属于多糖,在人体内水解转化为葡萄糖,也可为人类提供能量 |
| B、糖尿病患者吃糖量必须限制,但淀粉类食物不必进行限制 |
| C、同质量的脂肪在体内氧化放出的能量比糖类和蛋白质高得多,是提供能量的主要物质 |
| D、葡萄糖在人体内不可以转化为脂肪,所以吃糖不会使人发胖 |
根据表中信息判断,下列选项不正确的是( )
| 序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4 |
| ② | Cl2、FeBr2 | FeCl3、FeBr3 |
| ③ | KMnO4,HCl | Cl2、MnCl2… |
| A、第①组反应中,H2O2作还原剂 |
| B、第②组反应中,Cl2与FeBr2的物质的量之比为3:2 |
| C、第③组反应中,每生成1molCl2转移电子2mol |
| D、从三个反应可以得出:氧化性由强到弱顺序为MnO4->Fe3+>Cl2>Br2 |
 人体血液里Ca2+离子的浓度一般采用g/cm3来表示.抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度.某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度:
人体血液里Ca2+离子的浓度一般采用g/cm3来表示.抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度.某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度: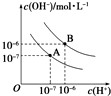 已知水在25℃(A)和T℃(B)时,其电离平衡曲线如图所示:
已知水在25℃(A)和T℃(B)时,其电离平衡曲线如图所示: