题目内容
8.在MnO2+4HCl═MnCl2+Cl2↑+2H2O 反应中氧化剂与还原剂分子数之比为( )| A. | 1:4 | B. | 1:2 | C. | 2:1 | D. | 1:1 |
分析 MnO2+4HCl═MnCl2+Cl2↑+2H2O中,Mn元素的化合价降低,Cl元素的化合价升高,以此来解答.
解答 解:MnO2+4HCl═MnCl2+Cl2↑+2H2O中,Mn元素的化合价降低,Cl元素的化合价升高,1molMnO2作氧化剂与2molHCl作还原剂转移电子相等,则氧化剂与还原剂分子数之比1:2,
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意氧化剂、还原剂的判断,题目难度不大.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
18.40gNaOH固体配成2L溶液,其物质的量浓度为( )
| A. | 0.5mol/L | B. | 5mol/L | C. | 10mol/L | D. | 20mol/L |
19.下列离子方程式的书写不正确的是( )
| A. | 氧化铝与盐酸反应:Al2O3+6H+═2Al3++3H2O | |
| B. | 氢氧化铝与NaOH溶液反应:Al(OH)3+OH-═AlO2-+2H2O | |
| C. | 向AlCl3溶液中滴加氨水:Al3++3OH-═Al(OH)3↓ | |
| D. | 向AlCl3溶液中加入过量NaOH溶液:Al3++4OH-═AlO2-+2H2O |
16. 无机化合物可根据其组成和性质进行分类
无机化合物可根据其组成和性质进行分类
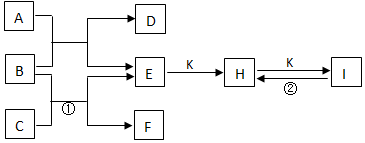
(1)如图所示的物质分类方法的名称是树状分类法.
(2)以Na、K、H、O、S、N中任两种或三种元素组成合适的物质,分别填在下表中②③⑥后面.
(3)写出⑦转化为⑤的化学方程式:CO2+2OH-=CO32-+H2O.
(4)写出实验室由⑩制备O2的化学方程式:2H2O2$\frac{\underline{\;二氧化锰\;}}{\;}$2H2O+O2↑.
(5)写出③与⑦反应的离子方程式2OH-+CO2=CO32-+H2O
(6)反应Cu+4HNO3(稀)═Cu(NO3)2+2NO2↑+2H2O中,用用单线桥法表示电子得失的方向和数目:
硝酸氧化剂:还原剂铜;若消耗19.2g Cu,则被还原HNO3是0.6mol,转移0.6NA个电子.
 无机化合物可根据其组成和性质进行分类
无机化合物可根据其组成和性质进行分类(1)如图所示的物质分类方法的名称是树状分类法.
(2)以Na、K、H、O、S、N中任两种或三种元素组成合适的物质,分别填在下表中②③⑥后面.
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①HCl②H2SO4 | ③NaOH ④Ba(OH)2 | ⑤Na2CO3 ⑥K2SO4 | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O2 |
(4)写出实验室由⑩制备O2的化学方程式:2H2O2$\frac{\underline{\;二氧化锰\;}}{\;}$2H2O+O2↑.
(5)写出③与⑦反应的离子方程式2OH-+CO2=CO32-+H2O
(6)反应Cu+4HNO3(稀)═Cu(NO3)2+2NO2↑+2H2O中,用用单线桥法表示电子得失的方向和数目:
硝酸氧化剂:还原剂铜;若消耗19.2g Cu,则被还原HNO3是0.6mol,转移0.6NA个电子.
13.设NA是阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | lmolAl3+离子含有的电子数为3NA | |
| B. | 7lgCl2约含有6.02×1023个筑原子 | |
| C. | 58.5g氯化钠固体中,含1 NA个阴离子 | |
| D. | 欲配制1.00L l.00mol/L的NaCl溶液,可将58.5gNaCl溶于1.00L水中 |
20.一定温度下在恒容的容器中发生如下反应:A(s)+2B(g)?C(g)+D(g),当下列物理量不发生变化时,能表明该反应已达到平衡状态的是( )
①混合气体的密度 ②混合气体的压强 ③混合气体的总物质的量 ④B的物质的量浓度.
①混合气体的密度 ②混合气体的压强 ③混合气体的总物质的量 ④B的物质的量浓度.
| A. | ①④ | B. | 仅②③ | C. | ②③④ | D. | 仅④ |
17.某元素基态原子的外围电子排布为3d54s2,则下列说法错误的是( )
| A. | 该元素为Mn元素 | B. | 该元素最高化合价为+7 | ||
| C. | 该元素属于d区元素 | D. | 该元素原子最外层共有7个电子 |
14.氢是一种重要的非金属元素.氢的单质及其化合物在科学研究和工业生产中有着广泛而重要的作用.
(1)工业上一般采用CO和H2反应合成可再生能源甲醇.反应如下:CO(g)+2H2(g)?CH3OH(g)△H=-90.1KJ•mol-1在250℃下,将一定量的CO和H2投入10L的密闭容器中,各物质的物质的量浓度(mol•L-1)变化如表所示:(前6min没有改变条件)
①x=0.14.
②250℃时该反应的平衡常数K的计算式为:$\frac{0.04}{0.06×0.1{2}^{2}}$ (不必化简).
③若6min~8min只改变了某一条件,所改变的具体条件是加1 mol氢气.
④第8min时,该反应是不是达到平衡状态不是.(填“是”或“不是”)
(2)某硝酸厂处理尾气中的NO的方法是用H2将NO还原为N2.已知:

H2还原NO生成氮气和水蒸气的热化学方程式是2NO(g)+2H2(g)═N2(g)+2H2O(g)△H=-665 kJ•mol-1.
(1)工业上一般采用CO和H2反应合成可再生能源甲醇.反应如下:CO(g)+2H2(g)?CH3OH(g)△H=-90.1KJ•mol-1在250℃下,将一定量的CO和H2投入10L的密闭容器中,各物质的物质的量浓度(mol•L-1)变化如表所示:(前6min没有改变条件)
| 2min | 4min | 6nin | 8min | … | |
| CO | 0.07 | 0.06 | 0.06 | 0.05 | … |
| H2 | x | 0.12 | 0.12 | 0.20 | … |
| CH2OH | 0.03 | 0.04 | 0.04 | 0.05 | … |
②250℃时该反应的平衡常数K的计算式为:$\frac{0.04}{0.06×0.1{2}^{2}}$ (不必化简).
③若6min~8min只改变了某一条件,所改变的具体条件是加1 mol氢气.
④第8min时,该反应是不是达到平衡状态不是.(填“是”或“不是”)
(2)某硝酸厂处理尾气中的NO的方法是用H2将NO还原为N2.已知:

H2还原NO生成氮气和水蒸气的热化学方程式是2NO(g)+2H2(g)═N2(g)+2H2O(g)△H=-665 kJ•mol-1.