题目内容
25℃时,0.1mol/L的NaB溶液的pH=8,将该NaB溶液与0.06mol/L的盐酸等体积混合(混合时溶液体积变化忽略不计),下列说法中不正确的是( )
| A、混合溶液中:c(HB)+c(B-)=0.05mol/L |
| B、混合溶液中:c(OH-)+c(B-)-c(H+)=0.04mol/L |
| C、该NaB溶液中:c(H+)+c(HB)=1.0×10-6mol/L |
| D、该NaB溶液中:c(Na+)-c(B-)=9.9×10-7mol/L |
考点:离子浓度大小的比较,盐类水解的应用
专题:盐类的水解专题
分析:25℃时,0.1mol/L的NaB溶液的pH=8,说明NaB为强碱弱酸盐,则HB为弱酸;将该NaB溶液与0.06mol/L的盐酸等体积混合后,混合液中含有0.03mol/L的HB、0.02mol/L的NaB,溶液显示酸性,
A.混合液中一定满足物料守恒,根据物料守恒进行解答;
B.根据电荷守恒可得:c(OH-)+c(Cl-)+c(B-)=c(H+)+c(Na+),则c(OH-)+c(B-)-c(H+)=c(Na+)-c(Cl-);
C.NaB溶液中水电离的氢离子与氢氧根离子浓度相等,根据质子守恒进行判断;
D.根据NaB溶液中的电荷守恒进行计算.
A.混合液中一定满足物料守恒,根据物料守恒进行解答;
B.根据电荷守恒可得:c(OH-)+c(Cl-)+c(B-)=c(H+)+c(Na+),则c(OH-)+c(B-)-c(H+)=c(Na+)-c(Cl-);
C.NaB溶液中水电离的氢离子与氢氧根离子浓度相等,根据质子守恒进行判断;
D.根据NaB溶液中的电荷守恒进行计算.
解答:
解:25℃时,0.1mol/L的NaB溶液的pH=8,说明NaB为强碱弱酸盐,则HB为弱酸;将该NaB溶液与0.06mol/L的盐酸等体积混合后,混合液中含有0.03mol/L的HB、0.02mol/L的NaB,溶液显示酸性,
A.根据混合液中的物料守恒可得:c(HB)+c(B-)=
×0.1mol/L=0.05mol/L,故A正确;
B.根据电荷守恒c(OH-)+c(Cl-)+c(B-)=c(H+)+c(Na+)可得:c(OH-)+c(B-)-c(H+)=c(Na+)-c(Cl-)=
(0.1mol/L-0.06mol/L)=0.02mol/L,故B错误;
C.该NaB溶液中,根据质子守恒可得:c(H+)+c(HB)=c(OH-)=
=1.0×10-6mol/L,故C正确;
D.根据NaB溶液中的电荷守恒可得:c(Na+)-c(B-)=c(OH-)-c(H+)=1.0×10-6mol/L-1.0×10-8mol/L=9.9×10-7mol/L,故D正确;
故选B.
A.根据混合液中的物料守恒可得:c(HB)+c(B-)=
| 1 |
| 2 |
B.根据电荷守恒c(OH-)+c(Cl-)+c(B-)=c(H+)+c(Na+)可得:c(OH-)+c(B-)-c(H+)=c(Na+)-c(Cl-)=
| 1 |
| 2 |
C.该NaB溶液中,根据质子守恒可得:c(H+)+c(HB)=c(OH-)=
| 1×10-14 |
| 1×10-8 |
D.根据NaB溶液中的电荷守恒可得:c(Na+)-c(B-)=c(OH-)-c(H+)=1.0×10-6mol/L-1.0×10-8mol/L=9.9×10-7mol/L,故D正确;
故选B.
点评:本题考查了离子浓度大小比较,题目难度中等,注意掌握溶液酸碱性与溶液pH的关系,明确判断溶液中离子浓度大小的方法,还要学会电荷守恒、物料守恒、质子守恒的应用.

练习册系列答案
相关题目
下列原子或离子的基态电子排布式正确的是( )
| A、Ni:[Ar]3d8 |
| B、Cu:[Ar]3d94s2 |
| C、S2-:[Ne]2s23p6 |
| D、Si:[Ne]3s23p2 |
下列关于实验原理、操作的叙述,不正确的是( )
| A、除去乙酸乙酯中的乙酸,可以用饱和的碳酸钠溶液 |
| B、配制溶液时,俯视刻度线来定容,会使得所配溶液浓度偏高 |
| C、用托盘天平称取8.7克食盐 |
| D、实验室可以用新制氢氧化铜悬浊液来检验甘油,观察到的现象是出现绛蓝色沉淀 |
已知0.1mol/L的碳酸氢钠溶液的pH为8.4,则下列说法正确的是( )
A、将该溶液加水稀释,
| ||
| B、加入少量KOH固体,钠离子和碳酸根离子浓度均增大 | ||
| C、c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) | ||
| D、c(Na+)=c(HCO3- )+2c(CO32-)+c(H2CO3) |
异丁烷的二氯代物共有(不考虑立体异构)( )
| A、5种 | B、4种 | C、3种 | D、2种 |
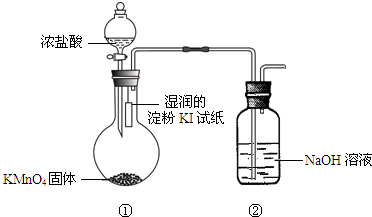 欲探究氯气与碘单质的氧化性强弱,某同学设计了如图装置(用浓盐酸和KMnO4固体反应制取氯气).
欲探究氯气与碘单质的氧化性强弱,某同学设计了如图装置(用浓盐酸和KMnO4固体反应制取氯气).