题目内容
2.下面的排序不正确的是( )| A. | 晶体熔点由低到高:CF4<CCl4<CBr4<CI4 | |
| B. | 硬度由大到小:金刚石>碳化硅>晶体硅 | |
| C. | 晶格能由大到小:NaF>NaCl>NaBr>NaI | |
| D. | 熔点由高到低:Na>Mg>Al |
分析 A.分子晶体的相对分子质量越大,熔沸点越大;
B.键长越短,共价键越强,硬度越大;
C.离子半径越小、离子键越强,则晶格能越大;
D.金属离子的电荷越大、半径越小,其熔点越大.
解答 解:A.分子晶体的相对分子质量越大,熔沸点越大,则晶体熔点由低到高顺序为CF4<CCl4<CBr4<CI4,故A正确;
B.键长越短,共价键越强,硬度越大,键长C-C<C-Si<Si-Si,则硬度由大到小为金刚石>碳化硅>晶体硅,故B正确;
C.离子半径越小、离子键越强,则晶格能越大,F、Cl、Br、I的离子半径在增大,则晶格能由大到小:NaF>NaCl>NaBr>NaI,故C正确;
D.金属离子的电荷越大、半径越小,其熔点越大,则熔点由高到低为Al>Mg>Na,故D错误;
故选D.
点评 本题考查元素周期律知识,侧重于学生的分析能力和基本概念的理解和运用的考查,注意元素的性质与对应单质、化合物的关系,把握元素周期律的递变规律是解答该类题目的关键,难度不大.

练习册系列答案
相关题目
13.下列措施或事实不能用勒沙特列原理解释的是( )
| A. | 滴加酚酞的氨水中加入氯化铵固体后红色变浅 | |
| B. | 棕红色的NO2加压后颜色先变深后变浅(已知:2NO2 (g)?N2O4 (g)) | |
| C. | 工业上生产硫酸的过程中,使用过量的空气以提高SO2的利用率 | |
| D. | 用硫酸氢钠去除暖水瓶中的水垢 |
10.据统计,金属腐蚀造成的损失远远超过火灾、水灾等自然灾害的总和,越来越被世界各国所重视,下面金属的防腐措施中,使用牺牲阳极的阴极保护法的是( )
| A. | 汽车底盘喷涂油漆 | B. | 掺防腐的金属制成不锈钢菜刀 | ||
| C. | 地下钢管连接锌块 | D. | 钢闸门连接电源负极 |
7.下列操作,发生“先产生沉淀,然后沉淀又溶解”现象的是( )
①金属钠投入到FeCl3溶液中
②向NaAlO2溶液中逐滴加入过量的稀盐酸
③澄清石灰水溶液中缓慢通入二氧化碳至过量
④向硅酸钠溶液中逐滴加入过量的盐酸.
①金属钠投入到FeCl3溶液中
②向NaAlO2溶液中逐滴加入过量的稀盐酸
③澄清石灰水溶液中缓慢通入二氧化碳至过量
④向硅酸钠溶液中逐滴加入过量的盐酸.
| A. | ①② | B. | ①③ | C. | ①④ | D. | ②③ |
14.下列变化过程中,没有发生化学变化的是( )
| A. | 铁的钝化 | B. | 光合作用 | C. | 碘的升华 | D. | 燃放烟花 |
11.下列离子方程式正确的是( )
| A. | 碳酸钙与醋酸反应:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 铁与氯化铁溶液反应:Fe+Fe3+═2Fe2+ | |
| C. | 碳酸氢钠溶液与氢氧化钠溶液混合:HCO3-+OH-═H2O+CO2↑ | |
| D. | 将氯气通入KBr溶液中:Cl2+2Br-═2Cl-+Br2 |
17.下列说法正确的是( )
| A. | 化合物 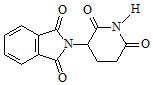 的分子式为C13H9O4N2 的分子式为C13H9O4N2 | |
| B. | CH3(CH2)2CH3与CH(CH3)3具有不同数目的一氯代物 | |
| C. | 在一定条件下,乙酸、氨基乙酸、蛋白质均能与NaOH发生反应 | |
| D. | 石油的裂化、裂解属于化学变化,煤的气化、液化则属于物理变化 |
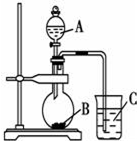 某研究性学习小组设计了一组实验验证元素周期律.
某研究性学习小组设计了一组实验验证元素周期律.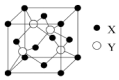 元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1;元素Y基态原子的3p轨道上有5个电子;元素Z的原子最外层电子数是其内层电子数的3倍;元素W基态原子的核外电子共有16种运动状态.
元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1;元素Y基态原子的3p轨道上有5个电子;元素Z的原子最外层电子数是其内层电子数的3倍;元素W基态原子的核外电子共有16种运动状态.