��Ŀ����
 ��ѧ��Ӧ�����ĸ�������������̽��̫��������������Ҫ��Դ��
��ѧ��Ӧ�����ĸ�������������̽��̫��������������Ҫ��Դ�����ڻ���ƽ�����װ�л�ԭ���£�N2H4����ǿ������H2O2�������ǻ��ʱ�������������ĵ�����ˮ���������ų��������ȣ���֪0.4molҺ̬�º�����Һ̬H2O2��Ӧ���ɵ�����ˮ����ʱ�ų�256.64kJ��������
��1��д���º�H2O2��Ӧ���Ȼ�ѧ����ʽ
��2����֪H2O��1��=H2O��g����H=+44kJ/mol����32gҺ̬��������˫��ˮ��Ӧ���ɵ�����Һ̬ˮʱ���ų���������
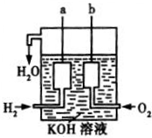
����������������ɴ���ʹ�õ�����ȼ�ϵ����һ�����͵�Դ���乹����ͼ��ʾ��a��b�����缫���ɶ��̼����ɣ�ͨ��������������ɿ�϶���ݳ������ڵ缫���淢���缫��Ӧ���ŵ磮
��3����缫�ֱ�Ϊa��
��4����缫��Ӧ�ֱ��ǣ�a����
���㣺ԭ��غ͵��صĹ���ԭ��
ר�⣺�绯ѧר��
������I����1��0.4molҺ̬�º�����Һ̬H2O2��Ӧ���ɵ�����ˮ����ʱ�ų�256.64kJ��������1molҺ̬����ȫ��Ӧ�ų�������=
=641.6kJ/mol��
��2��32g�µ����ʵ���=
=1mol��H2O��1��=H2O��g����H=+44kJ/mol�����ݸ�˹���ɼ�����ų���������
II����3��ȼ�ϵ���У�ͨ��ȼ�ϵĵ缫Ϊ������ͨ���������ĵ缫Ϊ������
��4������������ʧ���Ӻ����������ӷ�Ӧ����ˮ�������������õ��Ӻ�ˮ��Ӧ�������������ӣ���ط�Ӧʽ������ȼ�շ���ʽ��ͬ��
| 256.64kJ |
| 0.4mol |
��2��32g�µ����ʵ���=
| 32g |
| 32g/mol |
II����3��ȼ�ϵ���У�ͨ��ȼ�ϵĵ缫Ϊ������ͨ���������ĵ缫Ϊ������
��4������������ʧ���Ӻ����������ӷ�Ӧ����ˮ�������������õ��Ӻ�ˮ��Ӧ�������������ӣ���ط�Ӧʽ������ȼ�շ���ʽ��ͬ��
���
�⣺I����1��0.4molҺ̬�º�����Һ̬H2O2��Ӧ���ɵ�����ˮ����ʱ�ų�256.64kJ��������1molҺ̬����ȫ��Ӧ�ų�������=
=641.6kJ/mol�����Ȼ�ѧ��Ӧ����ʽΪN2H4��l��+2H2O2��l��=N2��g��+4H2O��g����H=-641.6kJ/mol��
�ʴ�Ϊ��N2H4��l��+2H2O2��l��=N2��g��+4H2O��g����H=-641.6kJ/mol��
��2��32g�µ����ʵ���=
=1mol��
N2H4��l��+2H2O2��l��=N2��g��+4H2O��g����H=-641.6kJ/mol�٣�
H2O��1��=H2O��g����H=+44kJ/mol�ڣ�
��-4���ڵ�N2H4��l��+2H2O2��l��=N2��g��+4H2O��l����H=-817��kJ/mol��
����1mol�º�˫��ˮ��Ӧ���ɵ�����Һ̬ˮ�ų�817.6kJ������
�ʴ�Ϊ��817��kJ��
II����3��ȼ�ϵ���У�ͨ��ȼ�ϵĵ缫Ϊ������ͨ���������ĵ缫Ϊ����������ͨ�������ĵ缫a�Ǹ�����ͨ�������ĵ缫b���������ʴ�Ϊ����������
��4������������ʧ���Ӻ����������ӷ�Ӧ����ˮ���缫��ӦʽΪH2-2e-+2OH-=2H2O�������������õ��Ӻ�ˮ��Ӧ�������������ӣ��缫��ӦʽΪO2+4e-+2H2O=4OH-����ط�Ӧʽ������ȼ�շ���ʽ��ͬ����ط�ӦʽΪ2H2+O2=2H2O��
�ʴ�Ϊ��H2-2e-+2OH-=2H2O�� O2+4e-+2H2O=4OH-��2H2+O2=2H2O��
| 256.64kJ |
| 0.4mol |
�ʴ�Ϊ��N2H4��l��+2H2O2��l��=N2��g��+4H2O��g����H=-641.6kJ/mol��
��2��32g�µ����ʵ���=
| 32g |
| 32g/mol |
N2H4��l��+2H2O2��l��=N2��g��+4H2O��g����H=-641.6kJ/mol�٣�
H2O��1��=H2O��g����H=+44kJ/mol�ڣ�
��-4���ڵ�N2H4��l��+2H2O2��l��=N2��g��+4H2O��l����H=-817��kJ/mol��
����1mol�º�˫��ˮ��Ӧ���ɵ�����Һ̬ˮ�ų�817.6kJ������
�ʴ�Ϊ��817��kJ��
II����3��ȼ�ϵ���У�ͨ��ȼ�ϵĵ缫Ϊ������ͨ���������ĵ缫Ϊ����������ͨ�������ĵ缫a�Ǹ�����ͨ�������ĵ缫b���������ʴ�Ϊ����������
��4������������ʧ���Ӻ����������ӷ�Ӧ����ˮ���缫��ӦʽΪH2-2e-+2OH-=2H2O�������������õ��Ӻ�ˮ��Ӧ�������������ӣ��缫��ӦʽΪO2+4e-+2H2O=4OH-����ط�Ӧʽ������ȼ�շ���ʽ��ͬ����ط�ӦʽΪ2H2+O2=2H2O��
�ʴ�Ϊ��H2-2e-+2OH-=2H2O�� O2+4e-+2H2O=4OH-��2H2+O2=2H2O��
���������⿼���Ȼ�ѧ��Ӧ��ԭ���ԭ����������֪ʶ�㶼�ǿ����ȵ㣬�ѵ��ǵ缫��Ӧʽ��д��Ҫ��ϵ������Һ�������д����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
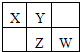 X��Y��Z��W��Ϊ������Ԫ�أ�������Ԫ�����ڱ��е�λ����ͼ��ʾ����Yԭ�ӵ������������Ǵ�����������3��������˵���в���ȷ���ǣ�������
X��Y��Z��W��Ϊ������Ԫ�أ�������Ԫ�����ڱ��е�λ����ͼ��ʾ����Yԭ�ӵ������������Ǵ�����������3��������˵���в���ȷ���ǣ�������| A������Ԫ�ص��⻯���У�Y���⻯��е���� |
| B��Z�ĵ��ʲ�����ˮ���ж���ͬ�������� |
| C�������ӵĻ�ԭ�ԣ�X��Y |
| D��X����̬�⻯������������������Ӧ��ˮ���ﷴӦ������ |