题目内容
下列说法正确的是( )
| A、等质量的铝分别投入过量的稀盐酸和NaOH溶液中,反应生成的气体在相同条件下体积相等 |
| B、金属单质与水反应都生成对应的碱和氢气 |
| C、活泼的金属或较活泼的金属都能与酸反应,但不能与碱反应 |
| D、由于钠比较活泼,所以它能从溶液中置换出金属活动顺序表中钠后面的金属 |
考点:常见金属的活动性顺序及其应用,钠的化学性质,铝的化学性质
专题:
分析:A、根据发生反应:2Al+3H2SO4=Al2(SO4)3+3H2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑进行计算;
B、碱金属单质,性质活泼,与水剧烈反应生成碱和氢气;
C、铝既能够与酸反应,又能与碱反应;
D、根据钠与盐溶液反应时,先与水反应,然后生成的碱再与盐反应或不反应.
B、碱金属单质,性质活泼,与水剧烈反应生成碱和氢气;
C、铝既能够与酸反应,又能与碱反应;
D、根据钠与盐溶液反应时,先与水反应,然后生成的碱再与盐反应或不反应.
解答:
解:A、由2Al+2NaOH+2H2O═2NaAlO2+3H2↑、2Al+6HCl═2AlCl3+3H2↑可知,2molAl分别与足量酸、碱反应都生成3molH2,则两份等量的铝粉分别与足量酸、碱反应生成等量的氢气,则相同状态下产生的气体体积之比是1:1,故A正确;
B、碱金属单质,性质活泼,与水剧烈反应生成碱和氢气,但大多数的金属和水不反应,故B错误;
C、铝为活泼金属,既能够与酸反应,也能与强碱反应,故C错误;
D、因钠与盐溶液反应时,先与水反应,然后生成的碱再与盐反应,所以它能从溶液中置换出金属活动顺序表中钠后面的金属,故D错误.
故选A.
B、碱金属单质,性质活泼,与水剧烈反应生成碱和氢气,但大多数的金属和水不反应,故B错误;
C、铝为活泼金属,既能够与酸反应,也能与强碱反应,故C错误;
D、因钠与盐溶液反应时,先与水反应,然后生成的碱再与盐反应,所以它能从溶液中置换出金属活动顺序表中钠后面的金属,故D错误.
故选A.
点评:本题主要考查了钠、铝等金属的性质、用途等知识,难度不大.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
某有机物的结构简式为HCOOCH2CH═CH2,它不具有的官能团是( )
A、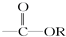 |
B、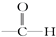 |
C、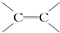 |
D、 |
某溶液中可能含有Na+、Al3+、Ba2+、SO42-、I-、S2-中的几种.分别取样进行以下实验:
①用pH计测试,溶液显弱酸性;②加新制氯水和淀粉溶液无明显现象.为确定该溶液的组成,还需检验的离子是( )
①用pH计测试,溶液显弱酸性;②加新制氯水和淀粉溶液无明显现象.为确定该溶液的组成,还需检验的离子是( )
| A、Na+ |
| B、SO42-,Na+ |
| C、S2-,SO42-,Na+ |
| D、Al3+ |
室温下在一定体积某浓度的Ba(NO3)2溶液中逐滴加入pH=1的稀硫酸至溶液中的Ba2+恰好完全沉淀时,测定溶液pH=2,若忽略两溶液混合时的体积变化,则稀硫酸的体积与Ba(NO3)2溶液的体积之比是( )
| A、1:10 | B、1:9 |
| C、10:1 | D、9:1 |
常温下,下列溶液中C(H+)最大的是( )
| A、pH=0的溶液 |
| B、0.04 mol?L-1H2SO4 |
| C、0.5 mol?L-1HCl |
| D、0.5 mol?L-1CH3COOH |
一定量的盐酸跟过量的铁粉反应时,为了减缓反应速度,且不影响生成氢气的总量,可向盐酸中加入适量的( )
| A、NH4Cl |
| B、KCl溶液 |
| C、NaNO3 |
| D、CH3COONa |