题目内容
8. 已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素.在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去).
已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素.在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去).请回答下列问题:
(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,则B的化学式可能是FeCl3;实验室制取A的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
(3)若A是NaOH,D是无毒气体,则反应②的离子方程式是Na2CO3+H2O+CO2═2NaHCO3.
(4)若A、C、D都是常见气体,C是导致酸雨的主要气体,则反应③的化学方程式为2H2S+SO2═3S↓+2H2O.
某同学将搜集到的一定量的酸雨保存在密闭容器中,每隔一定时间测酸雨的pH,发现在起始一段时间内,酸雨的pH呈减小趋势,用离子方程式解释原因:2H2SO3+O2═4H++2SO42-,.
分析 (1)D是生产、生活中用量最大、用途最广的金属单质,则D是铁,A可用于自来水消毒,A为Cl2,B为FeCl3,C为FeCl2;
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则A是NH3,B为NO,D为O2,C为NO2;
(3)若A是NaOH,D是无毒气体,则D为CO2,B为Na2CO3、C为NaHCO3;
(4)若A、C、D都是常见气体,C是导致酸雨的主要气体,应为SO2,则A为H2S,D为O2,B为S.酸雨的pH呈减小趋势,是因为亚硫酸被空气中的氧气氧化为硫酸,酸性增强.
解答 解:(1)D是生产、生活中用量最大、用途最广的金属单质,则D是铁,A可用于自来水消毒,A为Cl2,B为FeCl3,C为FeCl2,实验室制取氯气的离子方程式为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,
故答案为:FeCl3;MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则A是NH3,B为NO,D为O2,C为NO2,反应①的化学方程式为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,
故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(3)若A是NaOH,D是无毒气体,则D为CO2,B为Na2CO3、C为NaHCO3,反应②的离子方程式是:Na2CO3+H2O+CO2═2NaHCO3,
故答案为:Na2CO3+H2O+CO2═2NaHCO3;
(4)若A、C、D都是常见气体,C是导致酸雨的主要气体,应为SO2,则A为H2S,D为O2,B为S.反应③的化学方程式为:2H2S+SO2═3S↓+2H2O,
酸雨的pH呈减小趋势,是因为亚硫酸被空气中的氧气氧化为硫酸,酸性增强,反应的离子方程式为:2H2SO3+O2═4H++2SO42-,
故答案为:2H2S+SO2═3S↓+2H2O;2H2SO3+O2═4H++2SO42-.
点评 本题考查无机物推断,属于开放性题目,需要学生熟练掌握元素化合物知识,难度不大.

 快捷英语周周练系列答案
快捷英语周周练系列答案| A. | 3种 | B. | 5种 | C. | 7种 | D. | 9种 |
①沙粒和硫粉 ②硫酸钠和硫粉 ③铁屑和硫粉 ④木炭和硫粉.
| A. | 用水溶解并过滤 | B. | 加热使硫粉升华并过滤 | ||
| C. | 用CS2溶解并过滤 | D. | 用盐酸溶解并过滤 |

| A. | 沸腾炉 | B. | 接触室 | ||
| C. | 吸收塔 | D. | 三个设备中都有变 |
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
| A. | 乙炔分子比例模型: | B. | 乙烯分子的结构简式为CH2CH2 | ||
| C. | 一氯甲烷的电子式为: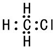 | D. | 2-甲基丁烷的键线式: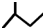 |
| A. | 周期表中金属与非金属的分界线附近可以找到半导体 | |
| B. | 周期表中F是最活泼的非金属,Li是最活泼的金属 | |
| C. | 元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共18个纵行 | |
| D. | X2+的核外电子数目为18,则X在第四周期第ⅡA族 |
| A. | 为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化 | |
| B. | 采取“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,可提高空气质量 | |
| C. | 铝及其合金是电气、工业、家庭广泛使用的材料,通常用电解氯化铝的方法制取铝 | |
| D. | DNOP(邻苯二甲酸二辛酯)是一种由邻苯二甲酸和正辛醇经酯化反应而得的一种酯类有机化合物,常用作增塑剂、溶剂以及气相色谱固定液,对人体无害,可用作食品添加剂 |
①m+4 ②m-4 ③m-8 ④m+2⑤m-6 ⑥m+12.
| A. | ①②③ | B. | ①④⑤⑥ | C. | ①②③④⑤ | D. | ①②③④⑤⑥ |